Регулация на обмяната на веществата
Обмяната на веществата в организма се различава в зависимост от функционалното състояние, в което се намира той – след нахранване или на гладно. Тя се различава по специфичното съотношение между хормоните, които регулират метаболизма, а оттам и доминирането на катаболитните (процесите на разграждане) или анаболитните (процесите на синтез) процеси в организма.
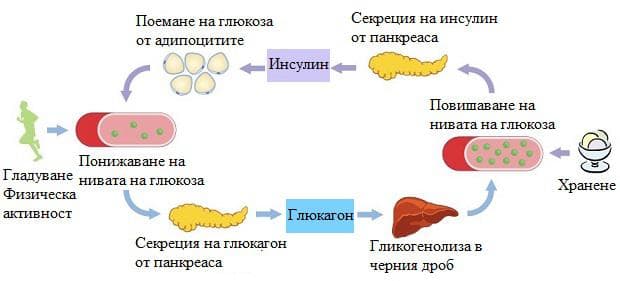
 След нахранване в кръвообращението постъпват елементарните съставки на основните хранителни вещества от храносмилателната система. Това води до повишаване на концентрацията на хормона на изобилието – инсулин. В черния дроб той насочва глюкозата към синтез на гликоген, потиска кетогенезата и глюконеогенезата. В мускулната и в мастната тъкан под влияние на инсулина глюкозния преносител 4 се включва в клетъчната мембрана. По този начин хормона на изобилието стимулира постъпването на глюкоза във вътреклетъчното пространство. Той увеличава експресията на гликолитичните ензими, а когато клетката няма нужда от повече енергия глюкозата се насочва към синтез на триацилглицероли и гликоген.
След нахранване в кръвообращението постъпват елементарните съставки на основните хранителни вещества от храносмилателната система. Това води до повишаване на концентрацията на хормона на изобилието – инсулин. В черния дроб той насочва глюкозата към синтез на гликоген, потиска кетогенезата и глюконеогенезата. В мускулната и в мастната тъкан под влияние на инсулина глюкозния преносител 4 се включва в клетъчната мембрана. По този начин хормона на изобилието стимулира постъпването на глюкоза във вътреклетъчното пространство. Той увеличава експресията на гликолитичните ензими, а когато клетката няма нужда от повече енергия глюкозата се насочва към синтез на триацилглицероли и гликоген.
 В състояние на гладно основна роля в регулацията има глюкагона. При липса на прием на хранителни вещества енергоразходът се осъществява само за сметка на ендогенните резерви. Глюкагонът стимулира гликогенолизата в черния дроб, а при по-дълготрайно гладуване и глюконеогенезата. В мускулните клетки липсва ензима глюкозо-6-фосфатаза. По тази причина глюкозо-6-фосфатът, получен от разграждането на резервния гликоген в мускулите, не може да напусне клетката и се използва само като източник на енергия. При продължително гладуване и изчерпване на мускулния гликоген в мускулите настъпва протеолиза, при което аминокиселините постъпват в циркулацията и достигат черния дроб, където се явяват субстрат за глюконеогенезата. Субстрат за гликонеогенезата е и глицеролът получен от разграждането на триацилглицеролите в мастната тъкан. Намаленият внос на въглехидрати и увеличеният катаболизъм на липидите водят до усилена кетогенеза. В много от тъканите кетоновите вещества (ацетоацетат, β-хидроксибутират и ацетон) се използват като източник на енергия – в миокарда, в мускулите дори и в мозъчните клетки. Мозъчните клетки са много чувствителни към евентуална хипогликемия. В тях липсват резерви от гликоген и ензими за глюконеогенеза. Те не могат да използват мастните киселини, защото не преминават кръвно-мозъчната бариера.
В състояние на гладно основна роля в регулацията има глюкагона. При липса на прием на хранителни вещества енергоразходът се осъществява само за сметка на ендогенните резерви. Глюкагонът стимулира гликогенолизата в черния дроб, а при по-дълготрайно гладуване и глюконеогенезата. В мускулните клетки липсва ензима глюкозо-6-фосфатаза. По тази причина глюкозо-6-фосфатът, получен от разграждането на резервния гликоген в мускулите, не може да напусне клетката и се използва само като източник на енергия. При продължително гладуване и изчерпване на мускулния гликоген в мускулите настъпва протеолиза, при което аминокиселините постъпват в циркулацията и достигат черния дроб, където се явяват субстрат за глюконеогенезата. Субстрат за гликонеогенезата е и глицеролът получен от разграждането на триацилглицеролите в мастната тъкан. Намаленият внос на въглехидрати и увеличеният катаболизъм на липидите водят до усилена кетогенеза. В много от тъканите кетоновите вещества (ацетоацетат, β-хидроксибутират и ацетон) се използват като източник на енергия – в миокарда, в мускулите дори и в мозъчните клетки. Мозъчните клетки са много чувствителни към евентуална хипогликемия. В тях липсват резерви от гликоген и ензими за глюконеогенеза. Те не могат да използват мастните киселини, защото не преминават кръвно-мозъчната бариера.
Съществува универсална сигнална система в клетките, която има много важна роля за превключване на метаболитните пътища в зависимост от функционалното състояние на клетката. Това е активираната от аденозинмонофосфат киназа (АМФК). Активността на тази система зависи от съотношението между АТФ/АМФ. Във всички случаи на изчерпване на запасите от АТФ – продължително гладуване, физическо усилие, хипогликемия, исхемия, АМФК насочва обмяната към алтернативни катаболни пътища и потиска анаболните процеси, свързани с разход на енергия.
 Хранителният прием е поведенчески акт. Той се регулира в резултат на взаимодействието на редица метаболитни, хормонални и други рефлексни стимули (вкус, аромат на храната, механорецепция в стомашно-чревния тракт). Тези фактори повлияват групи от неврони в хипоталамуса, които се означават като център на глада и център на ситостта. Към всички тези регулаторни механизми се прибавят и външни фактори, като присъщи за обществото и семейната среда навици, икономически възможности, професионална заетост. Хранителното поведение зависи от баланса между стимулиращите апетита (орексигенни) фактори – невропептид У и агути-свързан пептид, и инхибиращите приема на храна (анорексигенни фактори) – проопиомеланокртин. Невроните, които произвеждат основните регулатори на апетита, се повлияват от глюкорецепторите, които отчитат концентрацията на глюкозата в кръвта. Те се повлияват и от нивото на периферните хормони лептин, инсулин и грелин.
Хранителният прием е поведенчески акт. Той се регулира в резултат на взаимодействието на редица метаболитни, хормонални и други рефлексни стимули (вкус, аромат на храната, механорецепция в стомашно-чревния тракт). Тези фактори повлияват групи от неврони в хипоталамуса, които се означават като център на глада и център на ситостта. Към всички тези регулаторни механизми се прибавят и външни фактори, като присъщи за обществото и семейната среда навици, икономически възможности, професионална заетост. Хранителното поведение зависи от баланса между стимулиращите апетита (орексигенни) фактори – невропептид У и агути-свързан пептид, и инхибиращите приема на храна (анорексигенни фактори) – проопиомеланокртин. Невроните, които произвеждат основните регулатори на апетита, се повлияват от глюкорецепторите, които отчитат концентрацията на глюкозата в кръвта. Те се повлияват и от нивото на периферните хормони лептин, инсулин и грелин.
Регулация на апетита
Основните структури, които участват в регулацията на прием на храна, са хипоталамусът и продълговатият мозък. Хипоталамусът получава хормонални стимули от мастната тъкан и от стомашно-чревния тракт. Тези стимули носят информация за обема и на мастната тъкан и за обема и състава на приетата храна. Освен хипоталамуса и продълговатия мозък и други мозъчни структури играят роля в приема на храна. Например лимбичната система има отношение към процесите на търсене на храна и към емоционалните възприятия свързани с приема и.
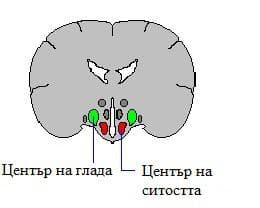
 Апетитът представлява желание за прием на храна и изпитване на удоволствие от храненето. Под глад обикновено се разбира ненаситно приемане на храна след дълъг период на гладуване. Ситостта е липса на желание на приемане на повече храна. Стимулирането на вентромедиалната зона на хипоталамуса предизвиква чувство за ситост, докато увреждането и води до непрекъснато приемане на храна. Стимулирането на латерално разположените структури води до ненаситно приемане на храна. По тази причина латерално разположените структури на хипоталамуса оформят центъра на глада, а вентромедиалните структури – центъра на ситостта. Тези центрове са свързани с регулацията на приема на храна.
Апетитът представлява желание за прием на храна и изпитване на удоволствие от храненето. Под глад обикновено се разбира ненаситно приемане на храна след дълъг период на гладуване. Ситостта е липса на желание на приемане на повече храна. Стимулирането на вентромедиалната зона на хипоталамуса предизвиква чувство за ситост, докато увреждането и води до непрекъснато приемане на храна. Стимулирането на латерално разположените структури води до ненаситно приемане на храна. По тази причина латерално разположените структури на хипоталамуса оформят центъра на глада, а вентромедиалните структури – центъра на ситостта. Тези центрове са свързани с регулацията на приема на храна.
Хранителното поведение се регулира от два основни механизма:
- глюкостатичен механизъм – в областта на вентромедиалните ядра на хипоталамуса се намират рецептори, които реагират на увеличението на концентрацията на глюкоза в кръвта. Това води до потискане на активността на центъра на глада. След края на абсорбцията на хранителните
 вещества в гастроинтестиналния тракт, концентрацията на кръвната захар намалява и това предизвиква чувство за глад. Увеличението на кръвната захар потиска апетита, докато намалението го активира. Глюкостатичният механизъм има значение за краткотрайната регулация на приема на храна. Активността на невроните, изграждащи центъра на ситостта, зависи от степента, в която те използват глюкозата. При слабо използване на глюкозата от тях, активността им намалява. Това води до надделяване на активността на центъра на глада и поява на чувство на глад. При увеличено използване на глюкоза от клетките на центъра на ситостта, неговата активност надделява и центъра на глада се потиска. При болните от захарен диабет концентрацията на глюкозата в кръвта е повишена, но количеството и в клетките е намалено. В клетките на вентромедиалните ядра концентрацията на глюкозата също е понижена, защото използването и е зависимо от инсулина. По тази причина при диабетно болните независимо от повишените нива на кръвната захар се наблюдава повишено чувство на глад.;
вещества в гастроинтестиналния тракт, концентрацията на кръвната захар намалява и това предизвиква чувство за глад. Увеличението на кръвната захар потиска апетита, докато намалението го активира. Глюкостатичният механизъм има значение за краткотрайната регулация на приема на храна. Активността на невроните, изграждащи центъра на ситостта, зависи от степента, в която те използват глюкозата. При слабо използване на глюкозата от тях, активността им намалява. Това води до надделяване на активността на центъра на глада и поява на чувство на глад. При увеличено използване на глюкоза от клетките на центъра на ситостта, неговата активност надделява и центъра на глада се потиска. При болните от захарен диабет концентрацията на глюкозата в кръвта е повишена, но количеството и в клетките е намалено. В клетките на вентромедиалните ядра концентрацията на глюкозата също е понижена, защото използването и е зависимо от инсулина. По тази причина при диабетно болните независимо от повишените нива на кръвната захар се наблюдава повишено чувство на глад.; - липолитичен механизъм – той има значение за регулацията на приема на храна за продължителни периоди от време, тъй като го съчетава с енергийния разход. По този начин
 липолитичния механизмъм участта в поддържането на постоянна телесна маса. Увеличението на запасите в мастните депа, стимулира центъра на ситостта. Центровете в хипоталамуса получават хормонални стимули от мастната тъкан, които носят информация за нейния обем. Мастните клетки не са само инертно енергийно депо – те имат и важна ендокринна функция. Произвеждат лептин, адипонектин, тумор некротизиращ фактор и резистин. Плазменото ниво на лептина отразява количеството мастна тъкан. Този хормон осигурява връзката между мастните клетки и хипоталамуса. Адипонектинът намалява образуването на глюкоза в черния дроб. Тумор некторизиращият фактор и резистинът намаляват чувствителността на прицелните клетки към инсулина. От всички тези хормони лепинът е този, който осъществява връзката с хипоталамуса. Той взаимодейства с лептинови рецептори. Отговорът от това взаимодействие е увеличаване на активността на симпатиковия дял на вегетативната нервна система, което се съпровожда с увеличаване на разхода на енергия, на двигателната активност, намаляване на приема на храна и на липогенезата и засилване на липолизата. Лептинът си взаимодейства с две групи неврони разположени в nucleus arcuatus в хипоталамуса. Това ядро се намира в близост до основата на третия вентрикул. Мястото е ключово, защото в него се осъществява приемането, обработването и интегрирането на постъпващата информация, необходима за поддържане на енергийната хомеостаза. В първата група неврони се потиска образуването на невропептид У и на норадреналин, които повишават апетита и стимулират приема на храна и потискат разхода на енергия. Лептинът потиска образуването на агути-свързания пептид, който представлява
липолитичния механизмъм участта в поддържането на постоянна телесна маса. Увеличението на запасите в мастните депа, стимулира центъра на ситостта. Центровете в хипоталамуса получават хормонални стимули от мастната тъкан, които носят информация за нейния обем. Мастните клетки не са само инертно енергийно депо – те имат и важна ендокринна функция. Произвеждат лептин, адипонектин, тумор некротизиращ фактор и резистин. Плазменото ниво на лептина отразява количеството мастна тъкан. Този хормон осигурява връзката между мастните клетки и хипоталамуса. Адипонектинът намалява образуването на глюкоза в черния дроб. Тумор некторизиращият фактор и резистинът намаляват чувствителността на прицелните клетки към инсулина. От всички тези хормони лепинът е този, който осъществява връзката с хипоталамуса. Той взаимодейства с лептинови рецептори. Отговорът от това взаимодействие е увеличаване на активността на симпатиковия дял на вегетативната нервна система, което се съпровожда с увеличаване на разхода на енергия, на двигателната активност, намаляване на приема на храна и на липогенезата и засилване на липолизата. Лептинът си взаимодейства с две групи неврони разположени в nucleus arcuatus в хипоталамуса. Това ядро се намира в близост до основата на третия вентрикул. Мястото е ключово, защото в него се осъществява приемането, обработването и интегрирането на постъпващата информация, необходима за поддържане на енергийната хомеостаза. В първата група неврони се потиска образуването на невропептид У и на норадреналин, които повишават апетита и стимулират приема на храна и потискат разхода на енергия. Лептинът потиска образуването на агути-свързания пептид, който представлява  ендогенен антагонист на рецепторите на α-меланоцитстимулиращия хормон, който потиска приема на храна. В други неврони лептинът стимулира образуването на проопиомеланокортинови продукти, които потискат приема на храна. Лептинът намалява приема на храна и увеличава енергийния разход чрез потискане на образуването на невропептид У и агути-свързания пептид и стимулира образуването на проопиомеланокортинови продукти. Група от неврони в латералния хипоталамус се повлияват от лептин-чувствителните клетки на nucleus arcuatus и синтезират меланин-концентриращия хормон. Други латерално разположени неврони произвеждат орексин, който стимулира приема на храна. Трета група неврони са чувствителни към промените в невропептид У и аглути-свързващия пептид. От латерално разположените хипоталамични нерони произлизат еферентни импулси, които координират поведенческите реакции, свързани с храненето.
ендогенен антагонист на рецепторите на α-меланоцитстимулиращия хормон, който потиска приема на храна. В други неврони лептинът стимулира образуването на проопиомеланокортинови продукти, които потискат приема на храна. Лептинът намалява приема на храна и увеличава енергийния разход чрез потискане на образуването на невропептид У и агути-свързания пептид и стимулира образуването на проопиомеланокортинови продукти. Група от неврони в латералния хипоталамус се повлияват от лептин-чувствителните клетки на nucleus arcuatus и синтезират меланин-концентриращия хормон. Други латерално разположени неврони произвеждат орексин, който стимулира приема на храна. Трета група неврони са чувствителни към промените в невропептид У и аглути-свързващия пептид. От латерално разположените хипоталамични нерони произлизат еферентни импулси, които координират поведенческите реакции, свързани с храненето.
В хипотамалусът се образуват четири орексигенни пептида, които увеличават апетита. Те са невропептид У, агути-свързан пептид, меланин-концентриращ хормон и орексин. Образуват се и два анорексигенни пептида (потискащи апетита) – α-меланоцитстимулиращ хормон и кокаин и амфетамин регулирания транскрипт.
 Единственият хормон в кръвта, който повишава апетита, увеличава телесното тегло и намалява окислението на мазнините, е грелинът. Той е антагонист на лептина. Освобождава се главно от клетките на стомашната лигавица, когато стомахът е празен. Плазмените нива на грелин са високи преди обичайното време на хранене и се понижават след прием на храна. Грелинът стимулира приема на храна посредством взаимодействие с рецепторите на хипоталамичните неврони, образуващи невропептид У.
Единственият хормон в кръвта, който повишава апетита, увеличава телесното тегло и намалява окислението на мазнините, е грелинът. Той е антагонист на лептина. Освобождава се главно от клетките на стомашната лигавица, когато стомахът е празен. Плазмените нива на грелин са високи преди обичайното време на хранене и се понижават след прием на храна. Грелинът стимулира приема на храна посредством взаимодействие с рецепторите на хипоталамичните неврони, образуващи невропептид У.
Nucleus tractus solitarii в продълговатия мозък е важен интегративен център, който регулира приема на храна. До него достигат импулси от механорецепторите на стомашната стена по вагусовите аферентни влакна. Разтягането на стомашната стена води до активирането на вагусовите ядра и невроните на nucleus tractus solitarii и до потискане на према на храна. Импулсите от разтягането на стомаха достигат и до центъра на ситостта в хипоталамуса. Качеството на храната също е от значение за създаване на чувството на ситост. Приемането на висококалорична храна създава по-силно чувство за ситост от приемането на нискокалорична храна. Това влияние притежава модулиращ характер и не е от съществено значение за регулиране на приема на храна.
Регулация на обмяната на въглехидратите
 Регулацията на обмяната на въглехидратите е свързана с поддържането на нивата на кръвната захар. Това се осъществява по няколко начина. Първият механизъм е свързан с глюкостатичната функция на черния дроб. В този орган се намира ензима глюкозо-6-фосфатаза, благодарение на който черния дроб може да осигури постъпването на необходимото количество глюкоза към плазмата. Това се осъществява чрез разграждане на чернодробния гликоген, активиране на ензимите за глюконеогенеза и получаване на глюкоза от невъглехидратни източници. Нивата на кръвната захар се регулират и по хормонални механизми. Инсулинът е единствения хормон, който понижава концентрацията на глюкоза в кръвта. Основните хормони, които му противодействат са глюкагон, адреналин, кортизол, растежен хормон и щитовидни хормони. Поддържането на кръвно-захарното ниво се осъществява чрез едновременното включване на сложни нервно-рефлексни и хормонални механизми.
Регулацията на обмяната на въглехидратите е свързана с поддържането на нивата на кръвната захар. Това се осъществява по няколко начина. Първият механизъм е свързан с глюкостатичната функция на черния дроб. В този орган се намира ензима глюкозо-6-фосфатаза, благодарение на който черния дроб може да осигури постъпването на необходимото количество глюкоза към плазмата. Това се осъществява чрез разграждане на чернодробния гликоген, активиране на ензимите за глюконеогенеза и получаване на глюкоза от невъглехидратни източници. Нивата на кръвната захар се регулират и по хормонални механизми. Инсулинът е единствения хормон, който понижава концентрацията на глюкоза в кръвта. Основните хормони, които му противодействат са глюкагон, адреналин, кортизол, растежен хормон и щитовидни хормони. Поддържането на кръвно-захарното ниво се осъществява чрез едновременното включване на сложни нервно-рефлексни и хормонални механизми.
Регулация на обмяната на белтъците
 В някои клетки в организма се откриват депа от въглехидрати и мазнини, но липсват такива от белтъци. Това означава, че в условия на енергиен дефицит се разграждат структурно и фукционално активни белтъци. По тази причина анаболитните и катаболитните процеси в белтъчната обмяна са много фино регулирани. Основните хормони, които вземат участие в регулацията са инсулин, соматотропен хормон и андрогенни стероиди. Инсулинът стимулира всички етапи от белтъчния синтез в мускулите, черния дроб и мастната тъкан. Растежният хормон има анаболен ефект в черния дроб, мускулите, вътрешните органи, костната и хрущялната тъкан. Част от ефектите му се осъществяват от инсулиноподобния растежен фактор. Катаболно действие върху белтъчната обмяна имат глюкокортикоидите и щитовидните хормони.
В някои клетки в организма се откриват депа от въглехидрати и мазнини, но липсват такива от белтъци. Това означава, че в условия на енергиен дефицит се разграждат структурно и фукционално активни белтъци. По тази причина анаболитните и катаболитните процеси в белтъчната обмяна са много фино регулирани. Основните хормони, които вземат участие в регулацията са инсулин, соматотропен хормон и андрогенни стероиди. Инсулинът стимулира всички етапи от белтъчния синтез в мускулите, черния дроб и мастната тъкан. Растежният хормон има анаболен ефект в черния дроб, мускулите, вътрешните органи, костната и хрущялната тъкан. Част от ефектите му се осъществяват от инсулиноподобния растежен фактор. Катаболно действие върху белтъчната обмяна имат глюкокортикоидите и щитовидните хормони.
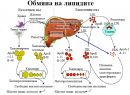
Регулация на обмяната на липидите
 Обмяната на липидите се регулира чрез взаимодействието на вегетативни, хормонални и паракринни влияния. Инсулинът играе централна роля в регулацията. След нахранване той стимулира постъпването на мастни киселини към мастната тъкан, скелетните мускули и миокарда. В адипоцитите той стимулира липогенезата. Адреналинът и глюкагонът притежават противоположно на инсулина действие. Те стимулират липолизата чрез повлияване на протеинкиназа А. Щитовидните хормони ускоряват липидния метаболизъм. Глюкокортикоидите стимулират липолизата и кетогенезата.
Обмяната на липидите се регулира чрез взаимодействието на вегетативни, хормонални и паракринни влияния. Инсулинът играе централна роля в регулацията. След нахранване той стимулира постъпването на мастни киселини към мастната тъкан, скелетните мускули и миокарда. В адипоцитите той стимулира липогенезата. Адреналинът и глюкагонът притежават противоположно на инсулина действие. Те стимулират липолизата чрез повлияване на протеинкиназа А. Щитовидните хормони ускоряват липидния метаболизъм. Глюкокортикоидите стимулират липолизата и кетогенезата.
От казаното до тук става ясно, че основна роля в регулацията на обмяната на веществата имат хормони, произвеждани от ендокринните жлези. По тази причина оптималното функциониране на ендокринната система е от ключово значение за нормалната обмяна на веществата.
Продукти свързани със СТАТИЯТА
УЕЙТ УЪРЛД L-КАРНИТИН капсули 1000 мг * 120
Библиография
https://courses.lumenlearning.com/wm-biology2/chapter/hormonal-regulation-of-metabolism/
http://courses.chem.indiana.edu/c483/documents/Lecturech19_000.pdf
https://chem.libretexts.org/Textbook_Maps/Biological_Chemistry/Metabolism/Metabolic_Pathways/MP4._Regulation_of_Metabolic_Pathways%3A_How_Is_It_Regulated%3F
Л. Витанова, Р. Гърчев; „Физиология на човека”; издателство АРСО
Arthur C. Guyton, M.D., John E. Hall, Ph.D.; „Text book of Medical Physiology“
СТАТИЯТА е свързана към
- Физиология на храносмилателната система
- Обмяна на веществата
- Десет шейка, които подобряват метаболизма и помагат да отслабнем
- Д-р Бойка Иванова Серафимова-Димитрова
- Продукти, които ускоряват обмяната на веществата
- Обмяна на белтъците
- Лофант, Анасонов исоп, Агастаче
- Обмяна на веществата
- Обмяна на липидите
- Отслабване с фурми според метаболизма
- Кучешко червено грозде, Дяволско грозде, Отровачка, Разваленка, Разгул
- Земна ябълка, Иерусалимски артишок, Гулия, Топинамбур



Коментари към Регулация на обмяната на веществата