Карцином in situ на други и неуточнени мъжки полови органи МКБ D07.6

Мъжката полова система се състои от няколко полови органи, които съставляват част от репродуктивния процес при мъжа.
Мъжките полови органи се делят на външни и вътрешни. Към външните спадат пениса и скротума (кожата около тестисите, нарича се още мъдница), докато вътрешните включват: простатна жлеза, семепроводни канали, семенник (тестис), семенно мехурче, надсеменник (епидидим), булбоуретрални жлези.
Подробна информация за анатомично устройство на мъжката полова система ще намерите при:
» Анатомия на мъжка полова система (systema genitalis masculina)
Подробна информация за карцином in situ на пенис може да намерите при:
» МКБ D07.4 Карцином in situ на пениса
Преканцерозните изменения в простатната жлеза са описани в:
» МКБ D07.5 Карцином in situ на простата
Преканцерозните състояния, които се разглеждат в МКБ D07.6 Карцином in situ на други и неуточнени мъжки полови органи, са:
- Карцином in situ на скротум (кожено-мускулната торбичка, в която се разполагат тестисите)
- Карцином in situ на тестис
- Карцином in situ на надсеменник (епидидим)
Описаните в това МКБ карциноми in situ на скротума са болест на Пейджет, екстрамамарна форма (Extramammary Paget’s disease) и болест на Боуен, засягаща скротума (Bowen's disease of the scrotum).
БОЛЕСТ НА ПЕЙДЖЕТ, ЕКСТРАМАМАРНА ФОРМА (Extramammary Paget’s disease)
Характерното място за развитие на болест на Пейджет е гърдата, по-специално на мамилата (зърното). Повече информация за болест на Пейджет на зърното може да намерите в:
Екстрамамарната (незасягаща млечната жлеза) форма на болестта е рядко срещан, бавно развиващ се кожен аденокарцином in situ, характеризиращ се с жлезна диференциация и коварно протичане. Състоянието може да е свързано или не със съпътстващо висцерално (произхождащо от вътрешните органи) злокачествено заболяване.
Заболяването включва предимно апокринните жлези (вид потни жлези) на кожата в областта на вулвата, скротума и перианалната област.
Патогенеза
Произходът на клетките на Paget е противоречив. Има четири различни теории, които обясняват четири различни модели на представяне:
- първата теория предполага, че стволови клетки, намиращи се в базалния клетъчен слой на епидермиса, се трансформират в клетки на Пейджет, като резултат на неправилното развитие на тези клетки до апокринни структури;
- според втората теория, епидермалните клетки на Paget произхождат от клетки, които са мигрирали от съседна злокачествена област — или от потните жлези на кожата, или друга съседна структура;
- третата теория предполага, че клетки на Paget могат да представляват форма на метастаза;
- свръхекспресия на HER2 протеин поради изключителна генна амплификация;
Изображение: Nephron, CC BY-SA 3.0, via Wikimedia Commons
Патоморфология
Хистопатологичните (хистопатология - микроскопско изследване на тъкан) особености на заболяването включват клетки на Пейджет (Paget’s cells), които са разположени поединично или в малки групи и имащи характерно оцветяване с хематоксилин и еозин.
Клетките на Paget са големи, слабо базофилни (синьо-виолетово оцветяване) и вакуолизирани (поява на вакуоли (мехурчета, което съдържа вода, електролити, въглехидрати и пигменти) в ядрото и цитоплазмата), имат големи ядра и често видими нуклеоли (ядърца, части от ядрото) с аморфна или гранулирана цитоплазма.
Клинична картина
Болест на Пейджет, екстрамамарна форма обикновено се появява като бавно нарастваща лезия, която може да бъде инвазивна или не.
Сърбежът в областта на скротума е единственото оплакване при повечето пациенти, въпреки че в някои от случаите има дразнене или обрив. При дългогодишни случаи може да има болка и кървене.
Първоначално лезията е зачервена, суха и повдигната, а по-късно може да се превърне в екзематоидна, разязвена, покрита с коричка или папиларна. Измененията са с резки очертания, имат плаки и отчетлив еритем (зачервяване).
Пациентите често дават анамнеза за продължително лечение с локални кортикостероиди и противогъбични препарати, преди диагнозата да бъде поставена чрез биопсия от мястото на увреждане.
Диагноза
Необичайно е да се постави диагноза клинично, затова се прави пънч-биоспия на засегнатата кожа, за да се получи достатъчно количество тъкан за изследване. Потвърждаването на диагнозата става чрез хистопатология и имунохистохимия (метод за определяне на различните видове клетки чрез свързване на антитела към определени части на клетката).
Оцветяването с хематоксилин и еозин при хистохимичния анализ обикновено помага за разграничаването на екстрамамарната форма на болестта на Пейджет от злокачествен меланом и болестта на Bowen. Клетките на Paget съдържат муцин и поради това се оцветяват положително с Алцианово синьо, алдехид фуксин, проба на Шиф (Schiff) и муцикармин.
Ако тези техники не дадат добър резултат, имунохистохимичното оцветяване за CAM 5.2 (маркер за кожен произход на образуванието), EMA (antiepithelial membrane antigen - антиепителен мембранен антиген), CK 7 (цитокератин 7) и GCDFP-15 (Gross Cystic Disease Fluid Protein-15) е полезно.
Клетките на Пейджет реагират положително с всички тези багрила и така се вижда жлезистата диференциация на тези клетки.
Изображение: www.myempd.com
Лечение
Лечението на карциномите in situ на скротума започва с първоначална клинична оценка, оценка за степента на разпространение на лезията и преценка дали има съпътстващ малигнен процес.
Хирургично лечение
Основното лечение при неинвазивната екстрамамарна форма на болестта на Пейджет е широката хирургична ексцизия (изрязване), защото така се избягва разпространението на болестта.
Локално лечение
Локалното лечение включва имиквимод 5% крем, който се използва всеки ден в продължение на 6 седмици. Фотодинамична терапия също може да се използва като ефективно лечение за това преканцерозно (предраково) изменение на скротума.
БОЛЕСТ НА БОУЕН, ЗАСЯГАЩА СКРОТУМА (Bowen's disease of the scrotum)
Това е необичайна форма на сквамозно (плоско)клетъчен карцином in situ, характеризиращ се с пигментни лезии, които клинично могат да имитират меланом, пигментиран базалноклетъчен карцином. Меланоцитен невус и себорейна кератоза.
Пациентите с ХИВ имат по-висок риск от развитие на плоскоклетъчен карцином in situ на кожата, поради повишения риск от инфекция с участието на човешки папилома вирус (HPV), която променя клетъчната пролиферация (увеличаване на броя на клетките) и апоптоза (програмирана клетъчна смърт).
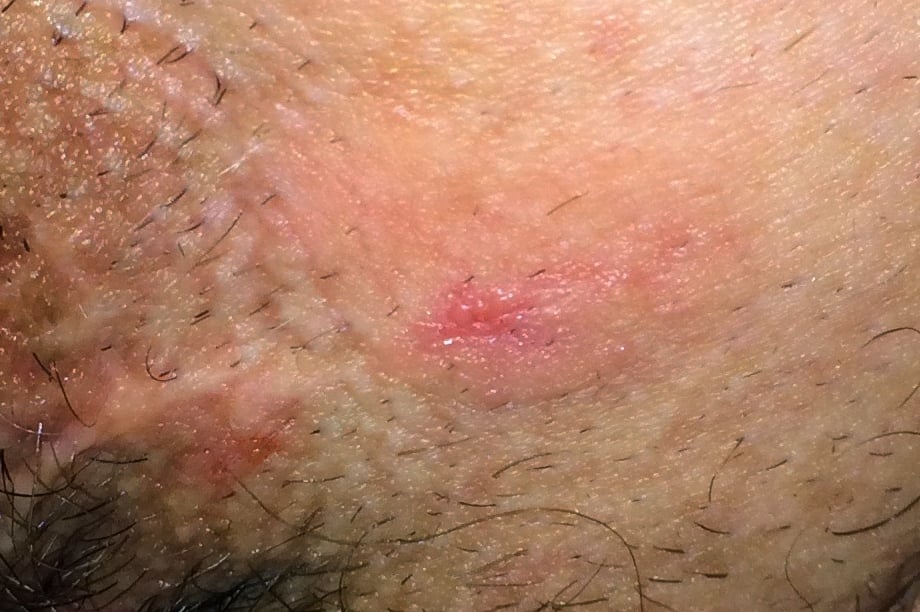
Клинична картина
Клинично лезията се представя като рязко ограничена, плоска, а понякога и разязвена пигментирана плака.
Няма стандартизирани дерматоскопски характеристики на болестта на Bowen, но чести находки са атипичните съдови структури, хомогенни зони от сивкаво-кафяви точки, подредени в линеен модел, както и неравномерно разпръснати възелчета.
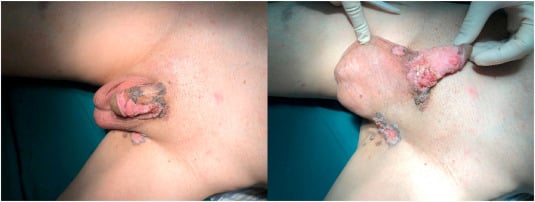
Изображение: www.sciencedirect.com
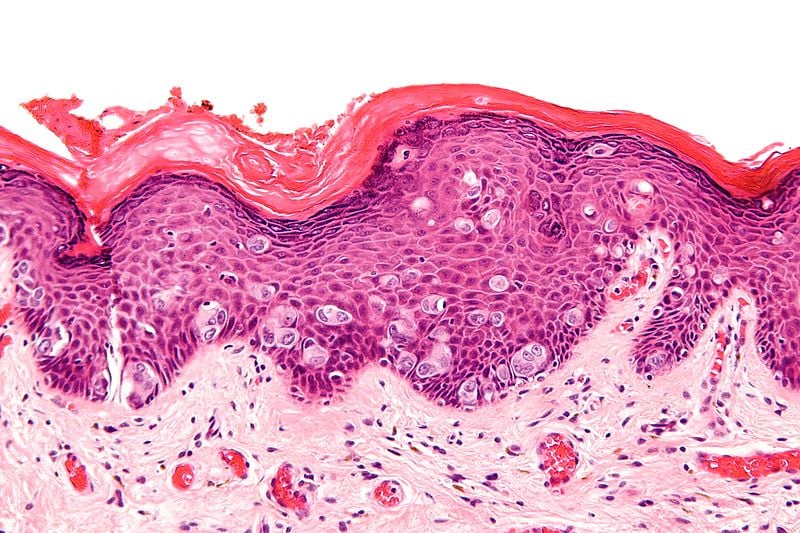
Патохистология
Хистологично, заболяването показва акантоза с дисплазия на цялата дебелина на епитела, нарушена кератинизация, множество клетки, съдържащи меланин, както и митотични фигури. Няма дермална инвазия. Отлагането на пигмент се обяснява с повишеното усвояване на меланин от диференцираните кератиноцити, а меланинът се произвежда от уголемени меланоцити в самия тумор.
Онкогенни човешки папилома вируси (главно HPV типове 16, 18, 31 и 33) са замесени в много случаи на плоскоклетъчен карцином in situ.
Установено е, че HIV-1 Tat протеин увеличава потенциала за репликация на клетки, инфектирани с HPV 16 и увеличава експресията на онкогени Е6 и Е7.
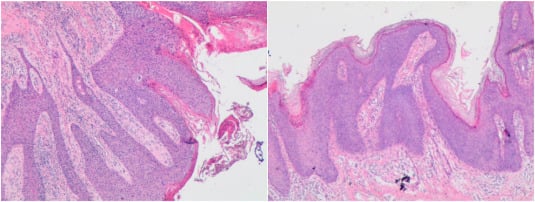
Изображение: www.sciencedirect.com
Лечение
Възможностите за лечение на пациенти с болестта на Bowen, засягаща скротума включват 5-флуороурацил 5% крем, имиквимод 5% крем, радиационна терапия или ексцизия (изрязване).
Прилага се и Mohs микрографска хирургия, тъй като чрез този метод се постига по-голямо съхранение на тъканите и се постига нисък процент на рецидивиране.
КАРЦИНОМ IN SITU НА ТЕСТИС
Ракът на тестисите се развива в единия или двата тестиса при млади мъже, но е възможно да се появи във всяка възраст. Това обикновено е лечим тип рак.
Тестисите имат две основни функции:
- произвеждат мъжките полови хормони (андрогени) като тестостерон;
- произвеждат сперматозоиди — мъжките клетки, необходими за оплождането на женската яйцеклетка. Сперматозоидите се произвеждат в дълги, подобни на нишки тръби в тестисите, наречени семенни каналчета, след което се съхраняват в надсеменника до тяхното узряване;
Тестисите се състоят от няколко типа клетки, всяка от които може да се развие в един или няколко вида рак. Важно е разграничаването на отделните видове карциноми, тъй като те се различават по начина, по който се лекуват и по тяхната прогноза. Двете основни групи клетки са герминативни и стромални клетки.
Повече от 90% от карциномите на тестиса се развиват в герминативните клетки. Това са клетките, които произвеждат сперматозоиди. Има два основни вида герминативноклетъчни тумори:
- семиноми;
- несеминоми;
Повече информация за карцинома на тестисите ще намерите при:
» МКБ C62 Злокачествено новообразувание на тестиса (ТУМОРИ НА ТЕСТИСИТЕ)
Патогенеза
Герминативноклетъчните карциноми на тестиса може да започнат като неинвазивна форма на болестта, наречена карцином in situ или интратубуларна герминативноклетъчна неоплазия, а клетките изглеждат необичайно под микроскоп, но те все още не са разпространени извън стените на семенните каналчета (мястото на образуване на сперматозоиди). Това заболяване невинаги прогресира до инвазивен рак.
В исторически план, терминът карцином in situ и тестикуларна интраепителна неоплазия са били използвани за описание на това преканцерозно състояние, но вече не се употребяват в литературата, тъй като тези лезии не притежават епителни характеристики. Предпочитания термин в съвременната литература е интратубуларна герминативноклетъчна неоплазия (ИТГКН).
Изображение: www.researchgate.net
Етиология
Един най-големите рискови фактори за развитие на интратубуларна герминативноклетъчна неоплазия е персоналната предразположеност към рак на тестисите, като пациенти с лична анамнеза за карцином на тестисите имат 25-кратно повишен риск от развитие на герминативноклетъчен рак в контралатералния (срещуположния) тестис.
Друг рисков фактор за развитие на заболяването е тестикуларната атрофия, при която има 4,3 пъти по-висок риск от положителни биопсии в тази група пациенти. Възрастта също е рисков фактор, като развитието на ИТГКН при пациенти под 30-годишна възраст е свързано със значителен риск от развитие на инвазивен карцином.
Инфертилитетът (безплодието) е значителен рисков фактор, тъй като се смята, че безплодието и рака на тестисите имат обща етиология (произход).
Пациенти с крипторхизъм (задържани тестиси) са 6,3-кратно повишен риск за развитие на карцином in situ.
Патоморфология
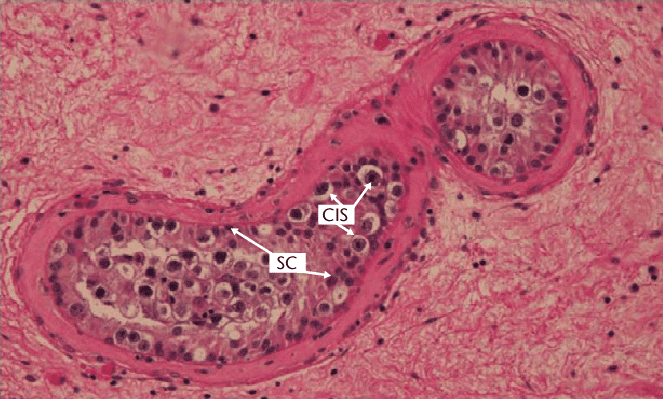
Патологичната морфология на интратубуларната герминативноклетъчна неоплазия е добре дефинирана и е подобна на тази при семином. Клетките при ИТГКН са по-големи от нормалните смерматогонии (първичните полови клетки при мъжете) и имат по-големи ядра с видни нуклеоли (ядърца, част от ядрото на клетката).
Цитоплазмата е богата на гликоген и съдържа PLAP (плацентарна алкална фосфатаза) ензим. Тези анормални клетки са разположени в базалната мембрана на семенните каналчета, където съдържанието варира от нормални клетки на Сертоли и смерматогонии до наличието изцяло на ИТГКН клетки.
Изображение: www.researchgate.net
Диагноза
Няма специфични методи или серумни туморни маркери за насочено диагностициране на интратубуларна герминативноклетъчна неоплазия.
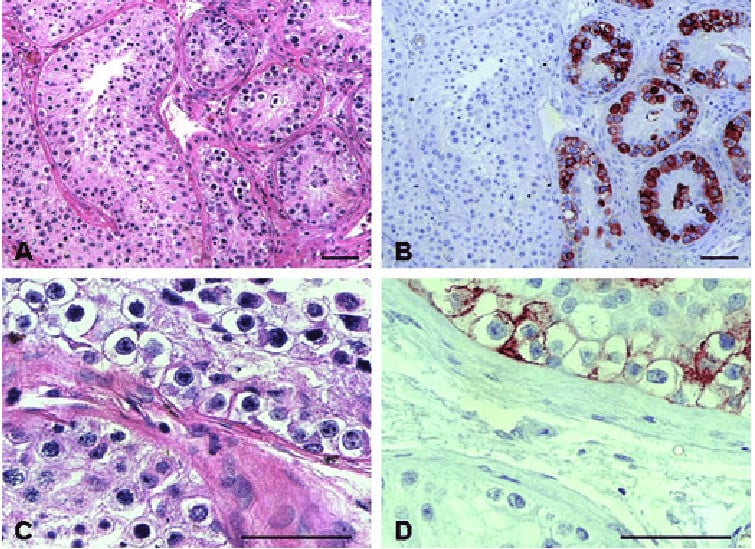
Имунохистохимичните маркери се използват рутинно при хистологично изследване, за да се подпомогне диагностицирането на интратубуларната герминативноклетъчна неоплазия. Най-често използваният маркер при имунохистохимия е PLAP, който има чувствителност 83-98%. Много добър за откриване на ИТГКН са Oct3/4 антителата, чиято чувствителност и специфичност са близо до 100%.
Отворената тестикуларна биопсия е инвазивна и има опасност за усложнения при и след провеждането й, ето защо е разработено откриване на променени клетки чрез анализ на спермата, въпреки че при този метод степента на откриване е значително по-ниска в сравнение с отворената хирургична биопсия.
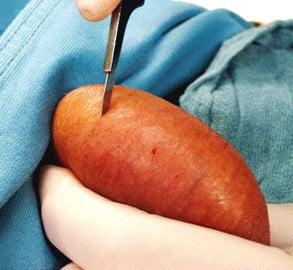 Тестикуларната биопсия е единственият надежден метод за диагностициране на ИТГКН. Материалът, взет при биопсия, трябва да бъде с размери поне 3x3 мм и да съдържа най-малко 30-40 каналчета, за да може да се направи качествено микроскопско изследване. Биопсичните проби трябва да бъдат поставени в разтвор на Boulin или Stieve, докато фиксирането с формалин трябва да се избягва, тъй като може значително да промени морфологията на тестикуларните клетки.
Тестикуларната биопсия е единственият надежден метод за диагностициране на ИТГКН. Материалът, взет при биопсия, трябва да бъде с размери поне 3x3 мм и да съдържа най-малко 30-40 каналчета, за да може да се направи качествено микроскопско изследване. Биопсичните проби трябва да бъдат поставени в разтвор на Boulin или Stieve, докато фиксирането с формалин трябва да се избягва, тъй като може значително да промени морфологията на тестикуларните клетки.
Усложненията, свързани с тестикуларната биопсия са основен проблем, което е и причината тази процедура да не се приеме за рутинно скринингово изследване. Общата честота на усложненията след извършена тестикуларна биопсия варира в интервала 3-20%.
Изображение: onlinelibrary.wiley.com
Лечение
Основната цел при лечението на интратубуларната герминативноклетъчна неоплазия е да се предотврати нейната злокачествена трансформация в тестикуларен герминативноклетъчен тумор. Съществуват четири възможности за лечение на ИТГКН:
- химиотерапия;
- радиотерапия;
- орхиектомия — хирургично отстраняване на тестисите;
- активно наблюдение на пациентите;
С изключение на наблюдението, останалите три опции съдържат значителен риск от безплодие, хипогонадизъм или и двете. Изборът на лечение се избира индивидуално, в зависимост от специфичните рискови фактори и желанията на пациента.
Други предракови изменения, включени в МКБ D07.6 Карцином in situ на други и неуточнени мъжки полови органи, са тези на надсеменника (епидидим), означавани още като:
ЕПИДИДИМАЛНА КРИБРИФОРМЕНА ХИПЕРПЛАЗИЯ (ЕКХ)
Епидидималната крибриформена хиперплазия е рядко срещан вариант на нормалната хистологична структура на епидидима, която се среща в около половината от хирургично премахнатите надсеменници.
Епидемиология
Туморът се появява в широк възрастов диапазон, средно 40-годишна възраст. Заболяването няма връзка с тестикуларната герминативноклетъчна неоплазия, аденоматозна хиперплазия на rete testis (мрежа от семенни каналчета в тестиса) или паренхимална атрофия.
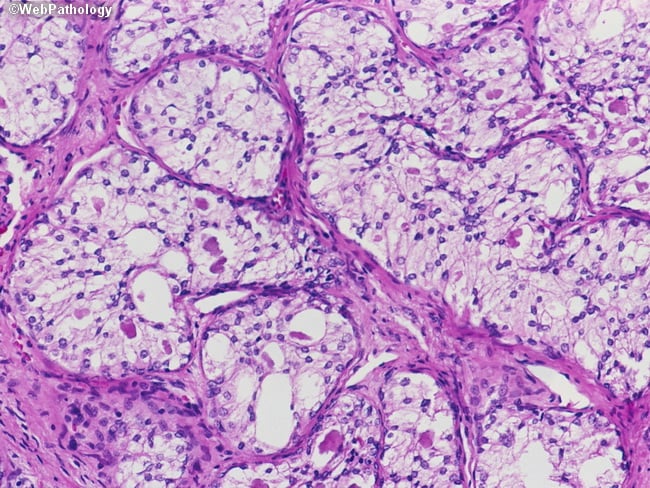
Изображение: www.webpathology.com
Патоморфология
Тази лезия се характеризира с епителни клетки, които имат нетипични хиперхромни (интензивно оцветени) ядра, вакуолизация (поява на вакуоли (мехурчета, което съдържа вода, електролити, въглехидрати и пигменти) в ядрото и цитоплазмата), образуване на формации в каналите на епидидима, рядко наблюдавана апоптоза (програмирана клетъчна смърт) и митотични (митоза — вид клетъчно делене) фигури.
За разлика от герминативните клетки, клетките при това заболяване не експресират алфа-фетопротеин, карциноембрионален антиген (CEA) или S-100 протеин. Ултраструктурно, клетките са плеоморфни (с различни форми) със стереоцилии (дълги ресни) в техните апикални (срещуположно на основата) граници и в каналчетата, като са разположени върху базална мембрана.
Крибриформената хиперплазия на епидидимите е много подобна на някои типове крибриформени интрадуктални карциноми in situ на млечната жлеза при жените и се характеризира със сложни клетъчни сводове и мостчета, които покриват разширените надсеменни каналчета.
Заглавно изображение: www.freepik.com
Коментари към Карцином in situ на други и неуточнени мъжки полови органи МКБ D07.6