Наследствена моторна и сетивна невропатия МКБ G60.0

Към това МКБ G60.0 Наследствена моторна и сетивна невропатия (НМСН), наречена още болест на Charcot-Marie-Tooth (СМТ) и перонеална мускулна атрофия, се включват голяма група от невропатии (увреждания на нервите), които се характеризират с въздействието си върху аферентните (по които постъпват импулси към мозъка) и еферентните (по които пренасят импулси от главния към гръбначния мозък) неврони.
При тези заболявания един или няколко компонента от периферната автономна или краниална (черепна)/спинална (гръбначномозъчна) система са увредени. В резултат на това засегнатите индивиди страдат от прогресивна мускулна атрофия и сензорна невропатия на крайниците.
Заболяването на Charcot–Marie–Tooth (CMT) представлява генетично и клинично хетерогенна група, характеризираща с прогресивна загуба на мускулна маса и усещането за допир в различни части от тялото.
Наследствената моторна и сетивна невропатия (НМСН):
Това е наследствено заболяване — ако един от родителите е болен от болестта на Charcot–Marie–Tooth, поколението му има 50% шанс също да развие болестта.
Наследствената моторна и сетивна невропатия е описана за първи път през 1886 от Charcot и Marie във Франция и от Tooth в Англия. Няколко години по-късно Dejerine и Sottas описват по-тежка, детска форма на наследствена невропатия.
Епидемиология
CMT засяга 1 човек на 2500 население като това е най-често срещаното заболяване на периферната нервна система.
Честотата на CMT 1 е 15 души на 100 000 население; честотата на CMT 1A е 10,5 души на 100 000 население, или 70% от CMT 1.
Честотата на CMT 2 е 7 души на 100 000 население.
Етиология
Болестта на СМТ е резултат от мутации, които причиняват дефекти в невроналните протеини.
Нервните импулси се провеждат от аксон (дълъг и тънък израстък на нервната клетка) с миелинова обвивка около него. Повечето мутации засягат миелиновата обвивка, но някои увреждат и аксона.
Най-честата мутация е дупликация (удвояване) на голям регион от късото рамо на хромозома 17, включваща гена PMP22.
Някои мутации засягат гена MFN2, който кодира митохондриален протеин. Клетките съдържат в ядрата и митохондриите си определен набор от гени. В нервните клетки митохондриите се придвижват по дължината на дългите аксони.
В някои от формите на заболяването, мутациите в MFN2 гена водят до образуване на големи участъци от митохондриите, които не могат да се придвижват по аксоните към синапсите, а това пречи на функционирането на синапсите.
Други клетки, които се срещат при заболяването на Charcot–Marie–Tooth, са Швановите клетки, които изграждат миелиновата обвивка чрез "обвиване" на плазмената им мембрана около аксона и образуване на структура, подобна на руло. Невроните, Швановите клетки и фибробластите заедно създаватфункциониращ нерв. Швановите клетки и невроните разменят помежду си молекулни сигнали, регулиращи развитието и диференциацията на нервните клетки.
При СМТ тези сигнали са прекъснати.
Ролята на миелиновите обвивки е свързана с по-бързото предаване на нервни импулси от нервните клетки. Когато миелиновата обвивка е увредена, нервните сигнали се предават по-бавно и това може да се установи чрез електромиография. Когато обаче е увреден аксона, това намалява акционния потенциал на мускула.
Клинична картина
Симптомите на перонеална мускулна атрофия обикновено започват в късното детство или в младежка възраст. Някои от болните не проявяват симптоми преди 30-40-годишна възраст.
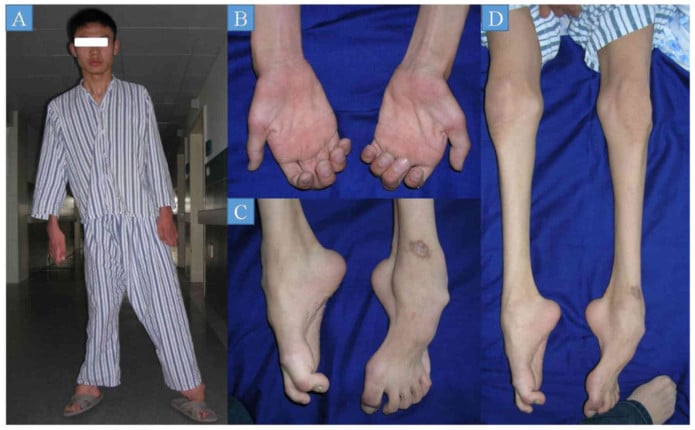
Най-често първи симптом е увисване на предната част на ходилото (drop foot). Може да се наблюдава и извиване на пръстите на краката.
Загубата на мускулна маса в долната част на краката може да даде на крака вид на "щъркелов крак'' или "обърната бутилка".
При прогресиране на заболяването може да се появи слабост в ръцете и предмишниците.
Загубата на усещането за допир в стъпалата, глезените и горната част на краката, а също и в ръцете, е характерно за различните варианти на перонеалната мускулна атрофия.
И ранните, и късните форми на заболяването се характеризират в "включване и изключване" на болезнени, спастични, мускулни съкращения, които могат да доведат до инвалидизация, когато заболяването се активира.
Класическа проява на заболяването са стъпалата с висок свод (пес кавус). Сензорните и проприоцептивните рецептори в ръцете и краката често са увредени, докато болковите рецептори (ноцицептори) са незасегнати.
Прекаленото използване на засегнатата ръка или крак може да активира симптоми, като скованост и болезнени мускулни крампи (схващания).
 www.spandidos-publications.com
www.spandidos-publications.com
При някои от пациентите може да бъде засегнато дишането, а също така и слуха, зрението, мускулите на врата и рамената.щ
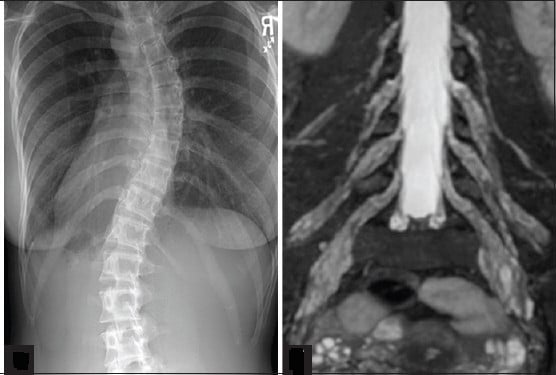
Често се наблюдава сколиоза (гръбначно изкривяване). Вероятни са проблеми от гастроинтестиналния тракт — затруднено дъвчене, преглъщане и говорене — причина е атрофия на гласните връзки.
Бременността и емоционалния стрес водят до влошаване на заболяването.
Пациенти с наследствена моторна и сетивна невропатия трябва да избягват продължителни периоди на обездвижване, тъй като имобилизацията значително засилва симптомите на НМСН.
Невропатичната болка (при увреждане на нервна структура) е чест симптом при заболяването на Charcot–Marie–Tooth. Болката може да бъде от силна до непоносима и пречи на ежедневните дейности.
Класификация
Според първоначалната класификация на болестта на Шарко-Мари-Тут, пациентите се разделят на две основни групи:
- Група 1 се е характеризирала ниска скорост на предаване на нервните импулси и данни за хипертрофична демиелинизараща невропатия;
- Група 2 се е характеризирала със сравнително нормална скорост на предаване на нервните импулси и с аксонална дегенерация;
През 1975 Dyck разширява класификацията:
- Charcot-Marie-Tooth (СМТ) типове 1А и 1В — доминантно — унаследени хипертрофични демиелинизиращи невропатии. Засегнатите пациенти се оплакват от слабост и атрофия в долната част на краката през юношеството, а по-късно развиват и слабост в ръцете. Това са най-често срещаните форми на заболяването;
- СМТ тип 2 — доминантно — унаследени сензорни невропатии. Започва през юношеството, като симптомите са подобни на тези при тип 1;
- СМТ тип 3 — хипертрофична невропатия при деца (Dejerine-Sottas). Началото е през детството и води до забавени двигателни умения;
- СМТ тип 4 - хипертрофична невропатия (болест на Рефсум), при която има натрупване на фитанова киселина. Харктеризира се с мускулна слабост и атрофия, както и при другите типове, но унаследяването е автозомно-рецесивно;
- СМТ тип 5 - свързана със спастична параплегия. Началото на проявите е между 5 и 12-годишна възраст. Първо се появява мускулна слабост и атрофия на долната част на краката, а след това и на горните крайници. При този тип се наблюдава и загуба на зрението и слуха;
- СМТ тип 6 - свързан с атрофия на зрителния нерв. Има ранно начало с мускулна слабост и атрофия, последвано от атрофия на зрителния нерв, водеща до загуба на зрението;
- СМТ тип 7 - наличие на ретинитис пигментоза (рядко заболяване, което атакува фоторецепторните клетки в окото и често води до слепота). Започва късно с мускулна слабост и атрофия основно в долните крайници;
Диагноза
Диагнозата се поставя въз основа на:
- клинично изследване
- измерване на скоростта на предаване на нервните импулси (чрез електромиография)
- биопсия на нерва
- образни изследвания:
При CMT тип 1A ултрасонографията с висока разделителна способност на срединния нерв (n. medianus) и други периферни нерви може да служи като допълнение към електродиагностиката.
При хората със CMT тип 1B се установяват по-големи срединни и блуждаещи нерви (nn. vagi), отколкото при здравите индивиди.
Ядрено-магнитен резонанс (ЯМР) на мускулите на долните крайници се използва за проследяване на прогресията на заболяването при пациенти с това заболяване.
 www.annalsofian.org
www.annalsofian.org
- ДНК тестове. ДНК тестовете могат да дадат окончателна диагноза, но още не са познати всички генетични маркери за наследствената моторна и сетивна невропатия.
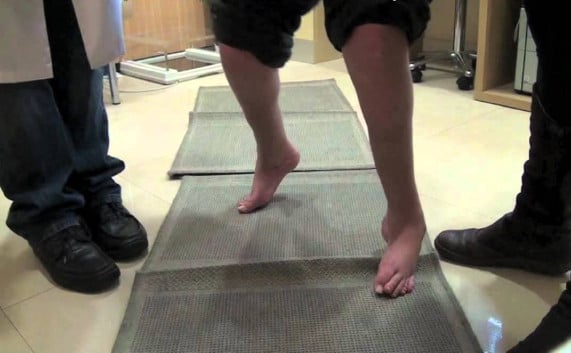
За да се установят белезите на мускулна слабост, пациентът трябва да върви на пети или да насочи част от крака си срещу сила с противоположна посока.
За да се определи дали има загуба на сетивност, трябва да се тестват дълбоките сухожилни рефлекси, които са намалени или отсъстващи при това заболяване.
Фамилната анамнеза също насочва към заболяването, тъй като заболяването на Шарко-Мари-Тут е наследствено. Липсата на фамилна анамнеза не изключва заболяване, но позволява изключването на други причини за невропатия, като диабет или излагане на някои химически вещества или лекарства.
Лечение
Все още не е разработено лечение за това заболяване, но се извършват експериментални изследвания с високи дози аскорбинова киселина (витамин С).
Много е важно пациентите със СМТ да поддържат мускулатурата си. Поради тази причина са препоръчани физиотерапия и умерена активност, но трябва да се избягва пренатоварване. Физиотерапевтът трябва да изготви програма за упражнения, която е строго индивидуална за всеки пациент. Нарушенията в походката могат да се коригират чрез специални ортези (протези).
Като крайно действие може да се предприеме хирургична интервенция, като пациентът избира дали да стабилизира краката си или да коригира прогресиращите проблеми.
Манипулациите включват изправяне и фиксиране на пръстите на краката, намаляване на свода на ходилото, а понякога и сливане на костите на глезенната става, за да се осигури стабилност.
Болните трябва да вземат допълнителни мерки срещу падане, защото фрактурите (счупванията) отнемат повече време за зарастване. Освен това, имобилизацията (обездвижването) по време на лечението на дадена фрактура може да влоши заболяването.
Прогноза
Прогнозите за различните CMT типове варират и зависят от клиничната тежест.
Като цяло перонеалната мускулна атрофия е бавно прогресираща невропатия, която може да доведе до инвалидизация вследствие на дисталната мускулна слабост и деформации.
Влошаването на двигателната активност на нервите при CMT 1A се засилва след 50-годишна възраст
В редки случаи засягането на n. phrenicus (диафрагмален нерв) може да е причина за затруднения с дишането.
Болестта на Шарко-Мари-Тут обикновено не съкращава очакваната продължителност на живота.
Превенция
Някои медикаменти (например винкристин, изониазид, паклитаксел, цисплатин и нитрофурантоин) причиняват увреждане на нервите и трябва да се избягват.
Асоцията "Charcot-Marie-Tooth" определя лекарството за химиотерапия - винкристин - като високорисково и опасно, като препоръчва избягването му от всички пациенти, болни от наследствена моторна и сетивна невропатия, включително и тези без симптоми.
Препоръчват се редовни физически упражнения в рамките на възможностите на индивида, като много хора остават физически активни.
Не се препоръчват специфични ограничения на активността.
Трябва да се избягва затлъстяването, защото затруднява ходенето.
Към МКБ G60.0 Наследствена моторна и сетивна невропатия (НМСН) спада и болестта на Дежерин-Сотас (Dejerine–Sottas), известна и като хипертрофична невропатия при деца.
Болест на Дежерин-Сотас (Dejerine–Sottas):
Заболяването носи името на Joseph Jules Dejerine и Jules Sottas - френски невролози, които го описали за първи път. Състоянието се характеризира с увреждане на периферните нерви и причинява прогресивна загуба на мускула маса
Етиология
Хипертрофичната невропатия при деца е резултат от генетични дефекти или в протеините, намиращи се в аксоните, или в протеините, съдържащи се в миелина.
По-конкретно мутациите са в MPZ, PMP22, PRX и EGR2 гените.
Заболяването се унаследява по автозомно-доминантен или автозомно-рецесивен път.
Клинична картина
Първоначалните прояви на наследствена моторна и сетивна невропатия започват през детството, обикновено преди 3-годишна възраст. Развитието на заболяването е забавено до тийнейджърска възраст, като след това може да прогресира и да предизвика тежка инвалидизация.
Симптомите при болестта на Dejerine–Sottas обикновено са по-тежки и бързо прогресиращи в сравнение с останалите форми на НМСН. Някои от пациентите не могат да ходят и запчват да използват инвалидна количка до края на първото си десетилетие, докато други болни имат нужда само от бастун, но през целия си живот.
Изтръпване, мравучкане или парене обикновено са първите симптоми.
Мускулната слабост обикновено първо се установява в задната част на крака, след което се разпространява и към предната група мускули.
Хипертрофичната невропатия при деца се характеризира с умерена до тежка слабост в горните и долните крайници, както и със загуба на сетивност, която се проявява предимно в долната част на краката, а също и в ръцете. Прогресирането на заболяването може да се прояви със загуба на мускулна маса и намаляване на мускулния тонус.
При влошаване на състоянието може да се появи слабост и в мускулите на ръката и предмишницата. Може да се развие дихателна недостатъчност.
 www.drfernandonoriega.com
www.drfernandonoriega.com
Други симптоми, които могат да се наблюдават при на болестта на Дежерин-Сотас, включвата:
- болка в крайниците
- изкривяване на гръбначния стълб
- деформация на пръстите тип "граблива птица"
- деформации на краката
- атаксия (липса на равновесие и координация)
- периферна арефлексия (забавени или липсващи рефлекси)
- бавно развитие на двигателните умение през детството.
По-рядко срещаните симптоми включват:
- намалени очни движения
- други очни проблеми, като нистагъм (спонтанно, нерегулируемо движение на очните ябълки) и анизокория (зениците имат различен диаметър)
- лека загуба на слуха.
Диагноза
Образната диагностика е основният начин за установяването на промени.
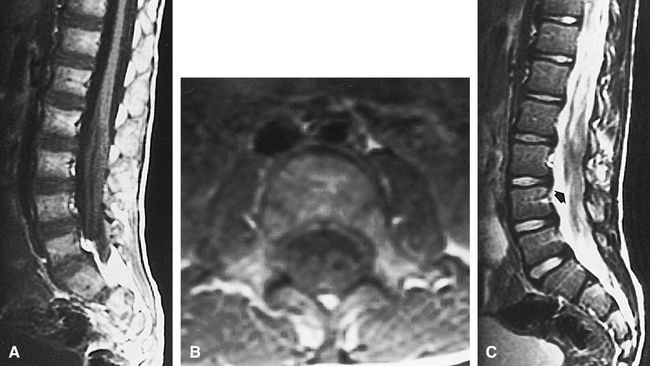
Ядрено-магнитен резонанс (ЯМР) е предпочитаният метод за образна диагностика, чрез който се определя степента на засягане на нервите.
Засегнатите нерви изглеждат удебелени поради хипертрофия на интерстициалната съединителната тъкан (придаващо на нервите особен вид на "лукова глава"), а също така се установява неврално и/или периневрално възпаление или филтрация.
Също така могат да бъдат засегнати лимфните възли около гръбначния стълб заедно с лимфните възли, разположени по хода на краниалните (черепно-мозъчните) нерви.
Електрофизиологичните изследванияпри синдрома на Дежерин-Сотас показват специфична полиневропатия, с наличието на демиелинизация на сензорните и моторните нервни влакна, което води до значително намаляване възбудимостта и на скоростта на провеждане на нервни импулси.
 www.ajnr.org
www.ajnr.org
Лечение
Няма специфично лечение на болестта на Dejerine–Sottas.
Терапията е поддържаща и насочена към облекчаване на симптомите.
Подходът към пациентите е мултидисциплинарен и включва специалисти по неврология, физиотерапия, ортопедия, трудова терапия.
Операции на глезена/стъпалото или специални обувки с добра опора на глезена могат да помогнат за коригиране или стабилизиране на ставите, свързани с ходенето.
За болката в мускулите може да се приема парацетамол или нестероидни противовъзпалителни лекарства (НСПВС).
Невралгията може да лекува с трициклични антидепресанти или други лекарства като карбамазепин или габапентин.
Генетичната консултация може да бъде полезна за семейства и лица с това заболяване.
Друго състояние от МКБ G60.0 е синдромът на Руси — Леви (Roussy–Levy).
Синдром на Руси — Леви (Roussy–Levy):
Това е рядко генетично заболяване, което причинява прогресивна загуба на мускулна маса. Причинява се от мутации в гените, кодиращи белтъци, които се необходими за функционирането на миелиновата обвивка на невроните, което от своя страна намалява скоростта на провеждане на нервните сигнали, а това води до ограничение в движението на мускулите.
Този синдром засяга деца и възрастни и се унаследява по автозомно-доминантен път. Няма известно лечение.
Заболяването е описано за първи път от Gustave Roussy и Gabrielle Levy.
Симптомите на заболяването са резултат от нервно увреждане и развилата се прогресивна мускулна атрофия. Неврологичното увреждане може да доведе до изчезване на сухожилните рефлекси (арефлексия), загуба на сетивност в дисталните сетивни влакна и намалена възбудимост на мускулите при стимулация с галваничен и фарадичен ток.
Прогресивната загуба на мускулна маса води до слабост в мускулите в долните крайници; атаксия (липса на равновесие и координация); пес кавус (вдлъбнато стъпало); постурални (свързани с позата) или статични тремори (треперене) на горните крайници; кифосколиоза (необичайно изкривяване на гръбначния стълб напред и настрани - кифоза, комбинирана със сколиоза); деформация на стъпалото.
Тези симптоми често водят до забавено начало в прохождането, загуба на координация и равновесие, увисване на предната част на ходилото и костни деформации на стъпалото.
Най-често симптомите при синдрома на Roussy–Levy се проявяват по време на детството и бавно прогресират до около 30-годишна възраст, когато при някои пациенти симптомите могат да отшумят.
Синдромът на Roussy–Levy е свързан с две генетични мутации - дупликация (удвояване) на PMP22 гена, който носи "инструкции" за продукцията на периферния миелинов протеин 22 - основен компонент на миелиновата обвивка. Другата мутация е миссенс-мутация (вид точкова мутация) в MPZ гена, който кодира миелинов протеин нула - основен структурен протеин на периферния миелин.
Неврологичното изследване установява намалена скорост на предаване на нервните импулси и хистологични особености на хипертрофична демиелинизираща невропатия. Електромиографията показва следи от леки неврогенни увреждания, докато биопсията на нерва показва формации тип "лукова глава".
Образуването на функциониращ нерв става с помощта на невроните, Швановите клетки и фибробластите. Между Швановите клетки и невроните се обменят молекулни сигнали, които регулират развитието и диференцирането на нервните клетки. При синдрома на Руси — Леви тези сигнали са прекъснати.
Клиничното изследване може да насочи към заболяването, докато потвърждаването на диагнозата става чрез генетични тестове, които целят откриването на мутации.
Синдромът на Roussy–Levy не води до смърт, а средната продължителност на живота е нормална. Поради прогресивната загуба на мускулна маса, обаче, пациентите може да се нуждаят от специално ортопедично оборудване или инвалидна количка.
Неврологичното изследване установява намалена скорост на предаване на нервните импулси и хистологични особености на хипертрофична демиелинизираща невропатия. Електромиографията показва следи от леки неврогенни увреждания, докато биопсията на нерва показва формации тип "лукова глава".
Образуваето на функциониращ нерв става с помощта на невроните, Швановите клетки и фибробластите. Между Швановите клетки и невроните се обменят молекулни сигнали, които регулират развитието и диференцирането на нервните клетки. При синдрома на Руси-Леви тези сигнали са прекъснати.
Клиничното изследване може да насочи към заболяването, докато потвърждаването на диагнозата става чрез генетични тестове, които целят откриването на мутации.
Синдромът на Roussy–Levy не води до смърт, а средната продължителност на живота е нормална. Поради прогресивната загуба на мускулна маса, обаче, пациентите може да се нуждаят от специално ортопедично оборудване или инвалидна количка.
Коментари към Наследствена моторна и сетивна невропатия МКБ G60.0
Zdr i as sm s sshtata diqgnoza i jiveq v Germaniq i tuka lekarite mi kazaha che vse oshte nqmalo lechenie za taq bolest preporchvat mi samo fizioterapiq