Ендокринна част на панкреаса МКБ D13.7
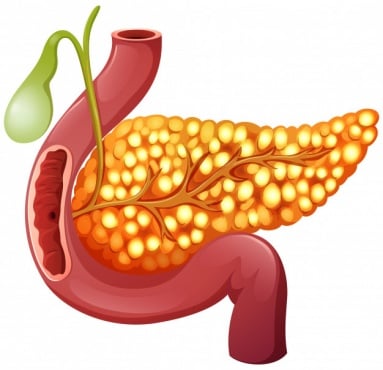
Панкреасът е орган, вземащ участие в храносмилателната и ендокринната система.
По-голямата част от панкреаса произвежда ензими, които спомагат за смилането на храната. Тази част се означава като "екзокринен панкреас".
Анатомична структура
Задстомашната жлеза също така съдържа и множество острови от ендокринни клетки, наречени "Лангерхансови острови". Тези острови съдържат малки кръгли клетки (ендокринни клетки), които произвеждат хормони, контролиращи нивото на кръвната захар — инсулин, глюкагон и соматостатин. Тази част от панкреаса се означава като "ендокринен панкреас".
Инсулинът понижава нивата на кръвната захар, докато глюкагонът има противоположно действие — повишава нивото на кръвната захар.
Подробна информация за панкреаса може да намерите при:
»Анатомия на задстомашна жлеза (pancreas)
В това МКБ D13.7 Ендокринна част на панкреаса са разгледани новообразуванията, засягащи ендокринната област на задстомашната жлеза, като тези неоплазми се наричат още тумори на островните клетки на панкреаса (островноклетъчни тумори), а също така и (добре диференцирани) панкреасни невроендокринни неоплазми.
Етиология
Голяма част от рисковите фактори, които водят до развитието на карцином на панкреаса, не са рискови фактори за развитие на островноклетъчни тумори/невроендокринни неоплазми на панкреаса.
Например тютюнопушенето удвоява риска за развитие на рак на панкреаса, но не изглежда да бъде фактор в развитието на тумори на клетките на Лангерхансовите острови.
Налице са няколко генетични (фамилни) синдроми, предразполагащи към развитието на невроендокринни неоплазми на панкреаса. За тези фамилни синдроми са характерни 3 неща:
- те са резултат на генетични промени, които могат да бъдат унаследени, тоест други членове на семейството могат да бъдат изложени на риск;
- тези генетични синдроми предразполагат (увеличават риска) към развитието на повече от един тип тумори;
- синдромите осигуряват информация за биологията на невроендокринните тумори на панкреаса, което ще позволи на учените могат да разберат клетъчните пътища, водещи до развитието на тези неоплазми, а оттам и разработването на по-добри методи за лечение;
Към фамилните синдроми спадат:
Множествена ендокринна неоплазия тип 1 (MEN-1)
Наследствен синдром, причинен от мутации в MEN1 гена, намиращ се в хромозома 11. MEN1 генът кодира протеина менин (menin), като пациентите с наследствена мутация в MEN1 гена са предразположени към развитието на тумори на хипофизната жлеза, паращитовидните (околощитовидни) жлези и панкреаса.
Синдром на фон Хипел-Линдау (von Hippel-Lindau, VHL)
Наследствен синдром, който се развива в резултат на наследствени мутации в гена за VHL, намиращ се в хромозома 3. Пациентите със синдром на фон Хипел-Линдау са предразположени към развитието на тумори в различни органи, включително мозъка (хемангиобластом), окото, бъбреците (бъбречно-клетъчен карцином) и надбъбречните жлези (феохромоцитом).
Първата проява на von Hippel-Lindau може да е заболяване на панкреаса, като повечето пациенти с това заболяване могат да развият тумор на панкреаса.
Туберозна склероза
Това е третият генетичен синдром, който предразполага към развитието на панкреасни невроендокринни неоплазми. Туберозната склероза се развива в резултат на наследствени мутации в един от двата гена — TSC1 или TSC2.
Генът TSC1 се намира в хромозома 9 и кодира протеина хамартин (hamartin).
Генът TSC2 се намира в хромозома 16 и кодира протеина туберин (tuberin).
При пациентите с туберозна склероза може да се наблюдава забавяне в развитието, умствено изоставане и дори аутизъм, като тези хора са предразположени към развитието на различни тумори.
Болните от туберозна склероза са предразположени към развитието на три различни мозъчни лезии:
- тубери (откъдето идва и името на заболяването);
- субепендимни (епендимът е тънка мембрана, подобна на епител, покриваща отвътре част от мозъчните структури) гигантоклетъчни астроцитоми;
- субепендимни нодули (възли).
Тези пациенти също така могат да развият характерни лезии по кожата (хипопигментни макули и фациални ангиофиброми), бъбреците (ангиомиолипоми), белите дробове (лимфангиолейомиоматоза), сърцето (рабдомиоми), както и очни тумори (хамартоми).
Повечето от тези лезии са изцяло доброкачествени новообразувания, като те могат да предизвикат симптоми в зависимост от тяхното местоположение.
Неврофиброматоза тип 1
Това заболяване е известно и като болест на фон Реклингхаузен (von Recklinghausen) и представлява наследствен синдром, който се развива в резултат на наследствени мутации в гена NF1, разположен в хромозома 17.
Генът NF1 кодира протеина неврофибромин (neurofibromin).
При пациентите с неврофиброматоза се появяват тъмни петна по кожата (тип кафе с мляко), както и доброкачествени и злокачествени тумори на нервната система (НС).
Към доброкачествените тумори на НС спадат неврофибромите, докато към злокачествените — злокачествен тумор на обвивката на периферните нерви.
При болестта на фон Реклингхаузен могат да се развият и характерни очни лезии, наречени нодули (възли) на Lisch, като в малък процент от случаите се развиват соматостатиноми на панкреаса/дуоденума.
Патогенеза
При някои пациенти е налице панкреасен тумор, имащ хистологичните характеристики на островноклетъчен тумор, но не се наблюдава повишаване на плазмените нива на хормоните.
Тези тумори се означават като нефункциониращи ендокринни тумори на панкреаса.
При част от пациентите нефункциониращите ендокринни неоплазми на панкреаса секретират панкреасен полипептид.
Панкреасният полипептид (PP) е продукт, представляващ маркер за ендокринните панкреасни тумори, но не е медиатор за специфичен РР-свързан синдром.
Други нефункциониращи ендокринни тумори на панкреаса вероятно секретират вещества, които имат малко или никакво клинично значение.
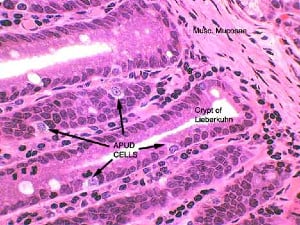 Клетките на ендокринните неоплазми на панкреаса се означават като APUD (amine precursor uptake and decarboxylation, захват и декарбоксилиране на аминови прекурсори) клетки, защото те са с високо съдържание на амини, могат да захващат аминовите прекурсори и съдържат ензима декарбоксилаза.
Клетките на ендокринните неоплазми на панкреаса се означават като APUD (amine precursor uptake and decarboxylation, захват и декарбоксилиране на аминови прекурсори) клетки, защото те са с високо съдържание на амини, могат да захващат аминовите прекурсори и съдържат ензима декарбоксилаза.
За първи терминът APUD е бил използван от Pearse (Пиърс) през 1968 година, за да се означат група от функционално и структурно подобни невроендокринни клетки, разположени на различни места в тялото.
Изображение:http://faculty.une.edu
Класификация
Островноклетъчните тумори могат да бъдат разделени на две основни групи:
- функциониращи (хормонално активни);
- нефункциониращи;
Повечето тумори на ендокринната част на панкреаса са функциониращи, тоест те секретират един или повече хормони в кръвта, което води до различни клинични прояви.
През 1927 година Wilder и сътрудници описват за първи път синдром, предизвикан от хормон-продуциращ панкреасен тумор, наблюдаван при пациент с хипогликемия и метастатичен островноклетъчен тумор, който причинява хипогликемията.
След това първоначално описание са били описани четири други синдроми, дължащи се на тумори на ендокринния панкреас.
Първият е синдром на Zollinger-Ellison (Цьолингер-Елисон), описан от Zollinger и Ellison през 1955 г.
Останалите три синдрома съставляват обща група и включват:
- синдром на Verner-Morrison (Вернер-Морисън);
- ВДХА (WDHA) синдром — водниста диария, хипокалиемия и ахлорхидрия;
- панкреасна холера (наричана още вазоактивен интестинален пептид [VIP]-секретиращ тумор или випом (VIPoma). Тези синдроми са описани от Verner и Morrison през 1958;
Третата група е синдром на глюкагонома, описан от Mallinson (Малинсон) през 1974 година.
Към четвъртата група спада синдромът на соматостатинома, описан от Ganda (Ганда) и Larsson (Ларсон) през 1977 година.
Клинична картина
Клиничните прояви при пациентите с тумори на ендокринния панкреас зависят от хормоните, секретирани от тумора. Това е и причината симптомите да варират при различните синдроми.
Видове тумори на ендокринната част на панкреаса
В това МКБ D13.7 Ендокринна част на панкреаса са разгледани следните новообразувания:
Инсулином
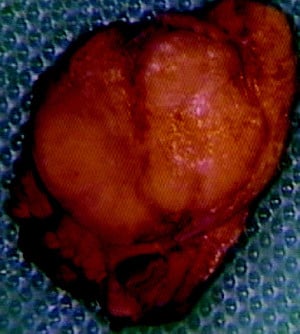 Инсулиномът е най-често срещаният ендокринен тумор на панкреаса и се характеризира с триадата на Whipple (Уипъл):
Инсулиномът е най-често срещаният ендокринен тумор на панкреаса и се характеризира с триадата на Whipple (Уипъл):
- симптоми на хипогликемия по време на гладуване;
- установяване на хипогликемия при изследване на кръвната захар;
- облекчаване на симптомите след прилагане на екзогенна глюкоза;
Симптомите включват:
- объркване;
- припадъци;
- замайване;
- промяна на личността;
- кома;
- сърцебиене;
- тремор;
- изпотяване;
- тахикардия;
В повечето случаи пациентите консумират богата на въглехидрати храна, за да облекчава или предотвратяване на тези симптоми.
Диагнозата на инсулинома се основава на изследването на глюкозата и инсулина в кръвта на всеки 4 до 6 часа, както и по време на възникването на симптомите.
При инсулином стандартните образни изследвания включват скенер (компютърна томография, КТ) на корем, ендоскопска ехография и висцерална ангиография.
Лечението на инсулином е хирургическо в почти всички случаи.
Изображение: Edward Alabraba et al., CC BY 2.0, via Wikimedia Commons
Незидиобластом
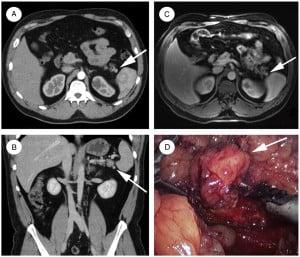 Незидиобластом е рядко срещан, инсулин секретиращ невроендокринен тумор на панкреаса.
Незидиобластом е рядко срещан, инсулин секретиращ невроендокринен тумор на панкреаса.
Тези лезии представляват хистологично доброкачествени новообразувания (аденоми), развитието на които е свързано с тежка, дългогодишна хипогликемия поради хиперинсулинизъм (високи нива на инсулин в кръвта).
Хирургичното отстраняване на тумора коригира проблемите с ниските нива на глюкозата.
Не съществуват точно определени дефиниции, които да определят разликата между инсулином и незидиобластом, като разграничаването им се основава на хистологичните особености на двата тумора.
Функционалната хипогликемия, наблюдавана при тези лезии, е също функция на незидиобластозата, при която е установена по-дифузна хиперплазия на панкреасните бета-клетки, които често с нехарактерен микроскопски вид.
Изображение: www.sciencedirect.com
Гастрином (синдром на Zollinger-Ellison)
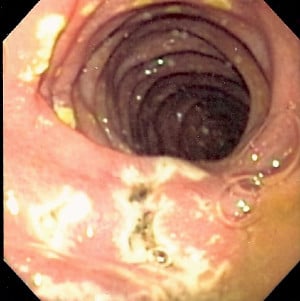 Гастриномите представляват новообразувания на ендокринния панкреас, отделящи големи количества от хормона гастрин в кръвта, който причинява стомашни или дуоденални язви.
Гастриномите представляват новообразувания на ендокринния панкреас, отделящи големи количества от хормона гастрин в кръвта, който причинява стомашни или дуоденални язви.
През 1955 година Zollinger и Ellison описват двама пациенти с тежка пептична язва и панкреасни ендокринни тумори, като смятат, че причината за язвените изменения са тези тумори.
Около 75% от гастриномите възникват спорадично (случайно), докато около 25% са свързани с MEN-1 синдрома.
Клиничните симптоми при пациенти с гастрином са пряк резултат от значително увеличените нива на циркулиращия гастрин.
Най-честите прояви при гастрином са коремната болка и пептичната язва на горния гастроинтестинален тракт, като се наблюдават при около 90-95% от пациентите със синдрома на Zollinger-Ellison.
Симптомите на пептичната язва при пациенти с гастрином са подобни на тези при пациенти с класическа пептична язва. Симптомите могат да бъдат и по-продължителни от тези при обикновена язва, като често не се поддават на стандартните медицински и хирургични терапии.
При около 60% от пациентите със синдрома на Zollinger-Ellison е налице дисфагия или одинофагия, или ендоскопски находки, отговарящи на рефлукс-езофагит.
При около една трета от пациентите с гастрином се наблюдава диария, която се развива вторично в резултат на голямото количество солна киселина в горния гастроинтестинален тракт и от преките ефекти на циркулиращия гастрин върху тънките черва.
В някои случаи диарията може да бъде единственият симптом при гастрином.
При някои хора с гастрином се развива вторично и стеаторея.
Клиничните прояви, които могат да насочат клиницистите към наличието на гастрином, са:
- наличие на множество язви;
- язви, които не се поддават към стандартно медикаментозно лечение;
- язва, която рецидивира след операция по случай язва;
- наличие на язва и диария;
- продължителна диария с неизвестна причина;
- фамилна анамнеза за пептична язва;
- фамилна анамнеза за MEN 1 синдром;
- язви при пациенти, при които не е налице инфекция с Helicobacter pylori и не съобщават за използването на нестероидни противовъзпалителни средства (НСПВС);
- повишени нива на гастрин, но без наличието на гастрином;
Изображение: http://en.wikipedia.org/wiki/User:Samir_%28The_Scope%29, CC BY-SA 3.0, via Wikimedia Commons
Вазоактивен интестинален пептид [VIP]-секретиращ тумор (випом, VIPoma)
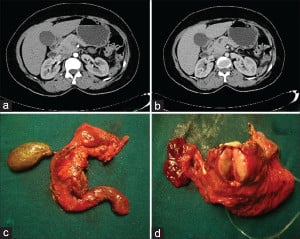 Симптомите при този тумор, наричан още синдром на Verner-Morrison (Вернер-Морисън) и ВДХА (WDHA) синдром (водниста диария, хипокалиемия, ахлорхидрия), са резултат от физиологичните ефекти, наблюдавани при свръхпроизводство на вазоактивен интестинален пептид от ендокринните неоплазми на панкреаса.
Симптомите при този тумор, наричан още синдром на Verner-Morrison (Вернер-Морисън) и ВДХА (WDHA) синдром (водниста диария, хипокалиемия, ахлорхидрия), са резултат от физиологичните ефекти, наблюдавани при свръхпроизводство на вазоактивен интестинален пептид от ендокринните неоплазми на панкреаса.
Основният симптом при пациентите със синдром на Verner-Morrison е воднистата диария, чийто прояви могат да бъдат постоянни, епизодични или периодични.
При пациентите с това заболяване често се наблюдават и коремни спазми.
Други симптоми, които се наблюдават при ВДХА синдрома, се развиват вторично в резултат на хипокалиемия, която пък се развива в резултат на загубата на калий с изпражненията.
Тези симптоми могат да включват мускулна слабост, сънливост и гадене.
Тъй като диарията при хората с такъв тумор се дължи на периодичната аденозин монофосфат-медиирана просекреторна гастроинтестинална стимулация, осъществена от VIP, терминът панкреасна холера се използва, за да се подчертае физиологичния механизъм на това заболяване.
Изображение: www.jpgmonline.com
Глюкагоном
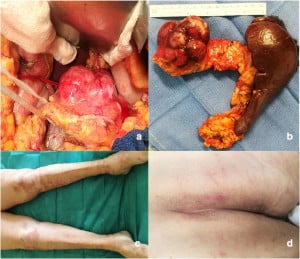 Глюкагономът секретира големи количества глюкагон и води до развитието на синдром, който се характеризира с:
Глюкагономът секретира големи количества глюкагон и води до развитието на синдром, който се характеризира с:
- дерматит;
- стоматит;
- загуба на тегло;
- анемия;
Дерматитът, който се наблюдава при глюкагоном, се нарича некротизиращ миграционен еритем и се характеризира с циклична промяна на мястото (миграция) на еритематозните петна, които се разпространяват серпигинозно (като серпентина) и след това демонстрират централна зона на възстановяване.
Хиперглюкагонемия (повишени нива на глюкагон в кръвта) при пациенти с глюкагоном води до нарушен глюкозен толеранс (т.е. диабет) и кахексия (дължаща се на анорексия и катаболитните ефекти на глюкагона), които да бъдат силно изразени, дори когато туморите са малки.
При около една трета от пациентите с глюкагоном са налице вторични тромбемболични състояния, поради което те могат да имат анамнеза за дълбока венозна тромбоза и/или белодробна емболия. Тази особеност прави глюкагонома уникален сред различните неоплазми на ендокринния панкреас.
Изображение: https://link.springer.com
Соматостатином
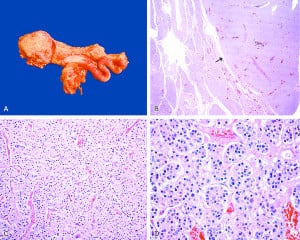 При тези новообразувания се наблюдават големи количества от хормона соматостатин в кръвта.
При тези новообразувания се наблюдават големи количества от хормона соматостатин в кръвта.
Соматостатиномите се срещат най-рядко спрямо останалите ендокринни неоплазми на панкреаса.
Симптомите при този тумор са резултат от общото инхибиращо действие на соматостатина върху действието на панкреаса, стомаха и червата, а именно:
- Пациентите със соматостатином често имат анамнестични данни за захарен диабет, което най-вероятно се дължи на инхибиторното (потискащото) действие на соматостатина върху секрецията на другите хормони на панкреаса — инсулин и глюкагон;
- Инхибиране действието на холецистокинина (невропептиден хормон, произвеждан от лигавицата на дванадесетопръстника) от соматостатина най-вероятно причинява холестаза (спиране оттичането на жлъчен сок от жлъчните пътища към червата) и образуването на камъни в жлъчния мехур;
Това инхибиране може да е отговорно за жлъчните колики, които често се наблюдават при пациенти със соматостатиноми; - Диария и/или стеаторея, като и двете могат да бъдат причинени от инхибирането на панкреасните ензими и секрецията на бикарбонати;
Триадата хипергликемия, камъни в жлъчката и стеаторея не е специфична за соматостатином, поради което пациентите с тези оплаквания трябва да бъдат изследвани за по-често срещани заболявания, преди да се подозира соматостатином.
По-голямата част от тези тумори се развиват в главата на панкреаса, като най-полезният метод за тяхното откриване и стадиране е компютърната томография (КТ) на корем.
Изображение: www.researchgate.net
Нефункциониращи островноклетъчни тумори
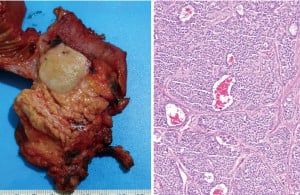 При голяма част от пациентите островноклетъчните не произвеждат хормони, поради което при тези лица не се наблюдават клинични прояви.
При голяма част от пациентите островноклетъчните не произвеждат хормони, поради което при тези лица не се наблюдават клинични прояви.
Тези тумори се означават като нефункциониращи панкреасни ендокринни неоплазми.
Нефункциониращите ендокринни неоплазми на панкреаса се характеризират с клинични прояви, дължащи се на обем заемащи формации в панкреаса, като:
- коремна болка;
- загуба на тегло;
- жълтеница;
Изображение: https://europepmc.org
Диагноза
При някои пациенти ендокринните неоплазми на панкреаса се откриват случайно, при изследване с КТ по друг повод.
Образна диагностика
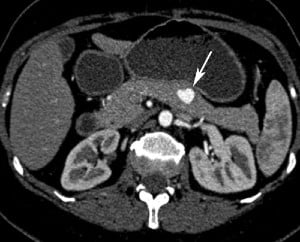 За първоначалното диагностициране на туморите на Лангерхансовите острови се препоръчва компютърна томография (КТ), като прецизността на този метод при локализирането на тумора се подобрява чрез използването на перорални и интравенозни контрастни вещества.
За първоначалното диагностициране на туморите на Лангерхансовите острови се препоръчва компютърна томография (КТ), като прецизността на този метод при локализирането на тумора се подобрява чрез използването на перорални и интравенозни контрастни вещества.
Ендокринните неоплазми на панкреаса се визуализират като солидни маси и показват богато кръвоснабдяване, което всъщност спомага за тяхното диагностициране.
Изображение: https://pubs.rsna.org
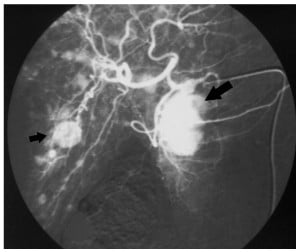 Ако чрез КТ не може да се открие първичния тумор, следващата стъпка в рентгенографската оценка може да бъде висцерална ангиография, при която се осъществява селективно визуализиране на артериалното кръвоснабдяване на панкреаса и перипанкреасните (в областта около панкреаса) зони.
Ако чрез КТ не може да се открие първичния тумор, следващата стъпка в рентгенографската оценка може да бъде висцерална ангиография, при която се осъществява селективно визуализиране на артериалното кръвоснабдяване на панкреаса и перипанкреасните (в областта около панкреаса) зони.
Изображение: www.mdpi.com
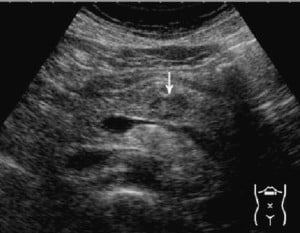
За визуализиране на туморите на панкреасните острови може да се използва ендоскопска ехография, като тази техника има предимството, че може едновременно да се направи и биопсия.
Изображение: www.sciencedirect.com
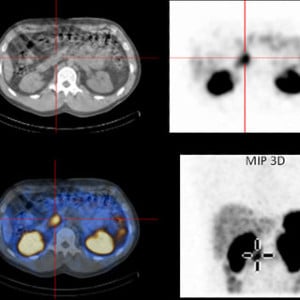 Друга метод за доказване на ендокринни тумори на панкреаса е визуализирането на соматостатиновите рецептори.
Друга метод за доказване на ендокринни тумори на панкреаса е визуализирането на соматостатиновите рецептори.
Тази техника се основава на наличието на такива рецептори при голяма част от ендокринните тумори на панкреаса, като има потенциал и за идентифициране и на тумори на черния дроб.
Изображение: www.researchgate.net
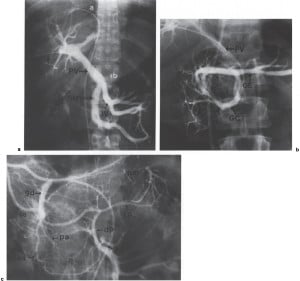 При малка част от пациентите с ендокринни неоплазми първичният тумор не може да се локализира чрез първоначално приложените методи за образна диагностика — КТ, висцерална ангиография и ендоскопски ултразвук, като това най-често се наблюдава при пациенти с много малък инсулином или гастрином.
При малка част от пациентите с ендокринни неоплазми първичният тумор не може да се локализира чрез първоначално приложените методи за образна диагностика — КТ, висцерална ангиография и ендоскопски ултразвук, като това най-често се наблюдава при пациенти с много малък инсулином или гастрином.
В тези случаи визуализацията на неоплазмите може да бъде да подпомогната чрез изследването на хормоните след селективна трансхепатална портална венозна проба, като при тази инвазивна техника се поставя катетър в кръвния поток.
Изображение: https://radiologykey.com
Лабораторни изследвания
Повишените нива на хормоните, произвеждани от ендокринните неоплазми, могат да бъдат изследвани в кръвта чрез специални тестове, при които се изследва кръвта на пациентите. За тези тестове се прилага имуноанализ, включително радиоимуноанализ.
Тестове за инсулин, гастрин, вазоинтестинален пептид, глюкагон, соматостатин, панкреасен полипептид, простагландини и други хормонални маркери обикновено се извършват в съответните референтни лаборатории.
Хистологично изследване
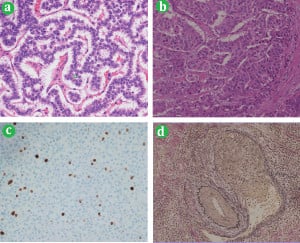 Хистологично, панкреасните ендокринни неоплазми имат специфичен вид. Тези тумори са склонни да образуват окръглени, добре демаркирани (разграничаващи се от околните тъкани) маси, което е в контраст с вида на злокачествените заболявания на панкреаса (аденокарциномите), при които не се наблюдава такова ясно отграничаване от околните тъкани.
Хистологично, панкреасните ендокринни неоплазми имат специфичен вид. Тези тумори са склонни да образуват окръглени, добре демаркирани (разграничаващи се от околните тъкани) маси, което е в контраст с вида на злокачествените заболявания на панкреаса (аденокарциномите), при които не се наблюдава такова ясно отграничаване от околните тъкани.
Когато нараснат, островноклетъчните тумори на панкреаса могат да прораснат в кръвоносни съдове, да излязат извън пределите на панкреаса и дори да засегнат съседни органи, например далака.
Панкреасните ендокринни неоплазми могат също така да се разпространят (метастазират) в лимфните възли и дори в други органи, като например в черен дроб, като всички тези особености ги доближават до злокачествените тумори.
Всички островноклетъчни тумори на панкреаса показват сходни характеристики при изследване със светлинен микроскоп.
Тези тумори са съставени от окръглени клетки с еднакви размери, съдържащи кръгли еднакви ядра.
Специален метод за оцветяване — имунохистохимично оцветяване — може да се използва за доказване производството на ендокринни хормони като инсулин и глюкагон в тъканните проби, взети при биопсии или от резецирани тумори.
Ранното хистологично изследване не предсказва клиничното поведение или ендокринните прояви на тези новообразувания.
Изображение: https://pancreas.imedpub.com
Лечение
По-голямата част от тези новообразувания са по-големи от 2 см, като лечението им е хирургично — панкреатикодуоденектомия (резекция по Уипъл) или дистална панкреатектомия (оперативното премахване на тялото и опашката на задстомашната жлеза).
Общият процент на 5-годишната преживяемост при всички пациенти с резецирани (резекция — изрязване) нефункциониращи неоплазми доближава 50%.
При пациенти с неоперабилни (които не могат да бъдат опериране) тумори е бил докладван частичен отговор при комбинирана химиотерапия.
Най-добър резултат (около 69%) е бил наблюдаван при пациентите, приемащи комбинацията стрептозоцин (streptozocin) + доксорубицин (doxorubicin).
Хирургичната резекция е основният метод за лечение при островноклетъчни тумори.
По време на хирургичното изследване (експлоративна лапаротомия) на туморите на ендокринна част на панкреаса се извършва и пълна оценка на панкреаса и региона около него. Черният дроб се изследва внимателно за наличието на метастази.
Изображение: www.freepik.com
Задължително се прави оценка на регионите извън панкреаса, при които има потенциална опасност за развитие на тумор:
- дуоденум (дванадесетопръстник);
- далак;
- тънки черва и техните кръвоносни съдове (мезентериум);
- лимфните възли около панкреаса;
- репродуктивния тракт при жените;
За идентифициране на тумора и получаване на допълнителна информация по време на операцията може да се използва ехография в реално време.
Ако е налице новообразувание, засягащо главата на панкреаса, може да се приложи процедура/операция на Уипъл (Whipple), а за тумори на опашката на панкреаса — дистална панкреатектомия.
Целите на хирургичната терапия при панкреасните ендокринни тумори включва:
- контрол на симптомите;
- внимателна резекция на туморната маса;
- запазване на колкото се може повече от паренхима на панкреаса;
Тъй като тези тумори нарастват много бавно, те често не се повлияват от конвенционална химиотерапия (която обикновено е насочена към бързо растящи клетки).
 Наскоро Администрацията за храните и лекарствените средства (FDA) на САЩ одобри лекарствата Sutent (сунитиниб, sunitinib) и Afinitor (еверолимус, everolimus) за лечение на напреднали ендокринни тумори на панкреаса.
Наскоро Администрацията за храните и лекарствените средства (FDA) на САЩ одобри лекарствата Sutent (сунитиниб, sunitinib) и Afinitor (еверолимус, everolimus) за лечение на напреднали ендокринни тумори на панкреаса.
Afinitor е одобрен за лечението на пациенти с прогресиращи невроендокринни тумори на панкреаса, които не могат да се отстранят хирургично.
Sunitinib спада към клас лекарства, означавани като "инхибитори на тирозин киназа", имащи ефект срещу кръвоносните съдове в туморите (антиангиогенно действие), както и срещу самия тумор (антитуморно действие).
В някои случаи тези медикаменти се използват за блокиране на симптомите, предизвикани от освобождаването на хормони от тумора.
Изображение: www.freepik.com
Прогноза
Прогнозата при тези тумори зависи от това дали те могат да бъдат или не отстранени по хирургичен път.
Други основни прогностични фактори при островноклетъчните тумори са:
- размера на тумора;
- наличието или липсата на инвазия на кръвоносните съдове;
- наличието или липсата на метастази в лимфните възли или други органи;
В повечето случаи процентът на оцеляване за 5-годишен интервал от време варира между 50 и 70%.
Заглавно изображение: www.freepik.com


Коментари към Ендокринна част на панкреаса МКБ D13.7