Аденокарцином на простатната жлеза
Аденокарциномът на простатната жлеза е малигнен тумор, който възниква в клетките на жлезата. Повечето клетки в простатната жлеза са от жлезист тип, което означава, че аденокарциномът е най-често срещаният вид злокачествен тумор, възникващ в простатната жлеза.
Злокачествени тумори на простатната жлеза имат характерна морфогенеза. Някои клинични наблюдения потвърждават значението на хормоните. Например нормалният растеж на простатата е под контрола на тестикуларния хормон тестостерон. Ранната, предпубертетна кастрация предпазва от развитие на нодуларна хиперплазия и от аденокарцином на простатната жлеза. Вече е доказано, че при болни с аденокарцином , в урината им се променя съотношението естрогени/андрогени в полза на естрогените. Нерядко аденокарциномът се развива на фона на една нодуларна, но най-вече на фона на атипична хиперплазия.
Патогенеза
Простатните аденокарциноми възникват от прекурсорни лезии, наречени пролиферативна възпалителна атрофия и простатна интраепителна неоплазия. Простатните интраепителни лезии, които се характеризират с епителни увреждания, регенерация и възпалителна клетъчна инфилтрация, се появяват в отговор на различни прокарциногенни натоварвания.
Наследствеността допринася значително за риска от развитие на аденокарцином на простатата. Откритите досега гени/локуси за възприемчивост включват RNASEL, кодиращ ензим, който действа като защита срещу вирусна инфекция, MSR1, кодиращ рецептор за бактерии в макрофагите и няколко места в хромозома 8. Постоянни изменения в експресията на ключови гени, свръхекспресия на MYC и AR и подрепресия на NKX3.1, PTEN, p27, GSTP1 и APC, съпътстват патогенезата на неоплазията.
Съкращаването на теломерните последователности повсеместно се появява рано по време на развитието на аденокарцином. Соматичните епигенетични промени, с хиперметилиране и транскрипционно заглушаване на няколко ключови гена, са най-разпространените и ранни аномалии на генома, очевидни при пролиферативна възпалителна атрофия и простатна интраепителна неоплазия.
Патологични характеристики
Простатният аденокарцином може да започне развитието си от всяка част на жлезата, но най-често началото е от задния дял на жлезата, който заедно с двата странични дяла образуват така наречената периферна зона. Макроскопски простатната жлеза е увеличена по размери, но невинаги и несилно. По-често се променя консистенцията. Жлезата става плътна, в резултат на дезмопластична реакция. Повърхността й е дребнозърниста. Срезната повърхност на жлезата показва, че туморната маса е с неясни граници, не е капсулирана и прораства в околната тъкан. Оцветката е белезникава.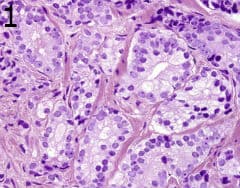
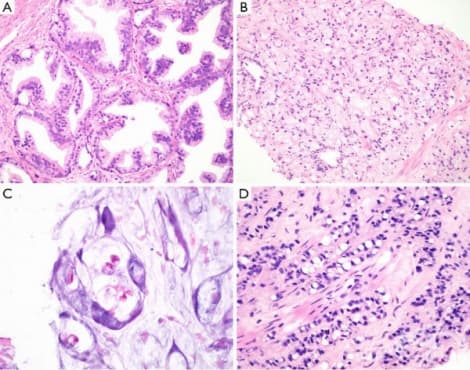
Повечето простатни аденокарциноми са съставени от ацини, подредени в един или повече модели. Диагнозата се опира на комбинация от архитектурни и цитологични находки. Светлинномикроскопските характеристики обикновено са достатъчни за диагностициране, но редки случаи могат да се възползват от имунохистохимични изследвания.
Архитектурните характеристики се оценяват при увеличение с ниска до средна мощност и включват вариация в ацинарното разстояние, размера и формата (фигура 1). Подреждането на ацини е диагностично полезно и е в основата на степента по Gleason. Злокачествените ацини обикновено имат неправилна случайна подредба, разпръсната в стромата в гроздове или единични ацини, обикновено с различие в разстоянието, с изключение на най-ниските степени на Gleason. Ацините в подозрителни огнища обикновено са с малък или среден размер, с неправилни контури, които стоят в контраст с гладките, кръгли до удължени контури на доброкачествени и хиперпластични ацини. Сравнението с прилежащите доброкачествени простатни ацини винаги е от значение. 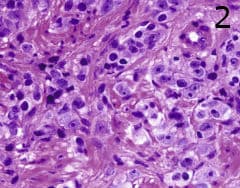 Промяната в ацинарния размер е особено полезен критерий, особено когато в периферията на фокус на добре диференциран карцином се наблюдават малки, неправилни абортивни ацини с примитивни лумени.
Промяната в ацинарния размер е особено полезен критерий, особено когато в периферията на фокус на добре диференциран карцином се наблюдават малки, неправилни абортивни ацини с примитивни лумени.
Стромата в аденокарцином на простатната жлеза често съдържа млад колаген, който изглежда леко еозинофилен, въпреки че десмоплазията може да е видна. Понякога вижда разцепване или изкривяване на мускулните влакна в стромата, но тази характеристика е непостоянна и ненадеждна сама по себе си.
Цитологичните особености на аденокарцином включват ядрено и нуклеоларно разширяване и те присъстват в по-голямата част от злокачествените клетки (фигура 2). Всяка клетка има нуклеол, така че се търси „видни“ ядра, които са с диаметър най-малко от 1,25 до 1,50 микрона. Идентифицирането на две или повече ядърца е практически диагностика на злокачествено заболяване, особено когато ядърцата са ексцентрично разположени в ядрото. Артефактите често затъмняват ядрата и нуклеолите, а преоценяването на ядра от хематоксилин създава един от най-често срещаните и трудни проблеми, срещани при тълкуването на подозрителни огнища. Разликите във фиксирането и боравенето с биопсичните проби влияят върху ядрения размер и хромазията, така че сравнението с клетки от един и същ образец е важно и служи като вътрешен контрол.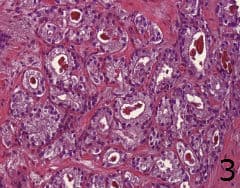
Киселинно сулфатиран и несулфатиран муцин често се наблюдава при ацини на аденокарцином. Муцинът се появява като аморфен или деликатен конец, слабо базофилни секрети в рутинни секции. Този муцин оцветява алциево синьо и се демонстрира най-добре при рН 2,5, докато нормалният епител на простатата съдържа неутрален муцин, реагиращ на ПАС. Киселинният муцин не е специфичен за карцином.
Кристалоидите са остри, иглоподобни еозинофилни структури, които често присъстват в лумените на добре диференциран и умерено диференциран аденокарцином (фигура 3). Те не са специфични за карцинома. Тези структури са резултат от нарушен метаболизъм на протеини и минерали в доброкачествените и злокачествените ацини и вероятно са свързани с твърдия еозинофилен протеинов секрет, който обикновено се намира в лумените на злокачествените ацини. Ултраструктурно, кристалоидите са съставени от електронноплътен материал, при който липсва периодичността на кристалите, а при рентгенографската микроанализа се открива изобилна сяра, калций и фосфор и малко количество натрий. Наличието на кристалоиди в метастатичен аденокарцином с неизвестно място на произход е силно предполагаеми доказателства за простатен произход, въпреки че е рядко срещана находка и не е категорична.
Колагенните микронудули са специфични, но рядко срещани и случайни находки при аденокарцином на простатната жлеза. Те се състоят от микроскопични нодуларни маси от пауцицелуларна еозинофилна фибриларна строма, която се нахвърля върху ацинарните лумени.
Периневралната инвазия е често срещана при аденокарцином и може да бъде единственото доказателство за злокачествено заболяване в биопсичните проби. Тази констатация е силно предположително доказателство за злокачествено заболяване, но рядко може да се прояви при доброкачествени ацини. Пълен растеж в периферията, интраневрална инвазия и ганглионна инвазия се срещат само при карцином.
Микросъдовата инвазия е силен индикатор за злокачествено заболяване и нейното присъствие корелира с хистологичната степен, въпреки че понякога е трудно да се разграничи от свързания с фиксацията артефакт на прибиране на ацини.
Библиография
https://www.sciencedirect.com/topics/medicine-and-dentistry/prostate-adenocarcinoma
https://www.mayoclinicproceedings.org/article/S0025-6196(11)61565-6/fulltext
https://healthengine.com.au/info/prostate-cancer-adenocarcinoma-of-the-prostate
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4784293/
http://www.pathologyoutlines.com/topic/prostateprostaticCAgeneral.html
Коментари към Аденокарцином на простатната жлеза