Карцином in situ с други уточнени локализации МКБ D09.7

В МКБ D09.7 Карцином in situ с други уточнени локализации се разглеждат две състояния:
- Синдром на Мюр-Тор (Muir-Torre syndrome)
- Миелопролиферативни неоплазми (новообразувания).
Синдром на Мюр-Тор (Muir-Torre syndrome)
› Диагноза
› Лечение
Миелопролиферативни неоплазми
› Диагноза
› Лечение
Синдром на Мюр-Тор (Muir-Torre syndrome)
През 1967 година Muir и Torre съобщават за пациенти с множество кожни тумори, заедно с висцерални злокачествени заболявания. Синдромът на Muir-Torre (MTS) е комбинация от неоплазми на кожата (обикновено себацеен (на мастните жлези — glandulae sebaceae) аденом, себацеен епителиом или себацеен карцином, а също и кератоакантома) и висцерални (на вътрешните органи) злокачествени заболявания (на ректума, ендометриума (лигавицата на матката), тънките черва и др.).
MTS има автозомно-доминантен модел на унаследяване при 59% от случаите, висока степен на засягане и с променливи прояви.
Синдромът на Мюр-Тор се счита за подтип на наследствения неполипозен колоректален карцином. Заболяването е свързано с наследствен дефект при репарация (поправка) на неправилно сдвоени бази от копие на ДНК (DNA mismatch repair), което води до микросателитна (микросателити - повтарящи се участъци от ДНК) нестабилност, наблюдавана в около 70% от туморите.
Епидемиология
Синдромът на Muir-Torre се наблюдава и при двата пола, средната възраст на развитие е 53 години.
При около 50% от пациентите може да се наблюдава положителна фамилна анамнеза за MTS. Кожните неоплазми могат да предхождат или да следват развитието на висцерално злокачествено заболяване.
Клинична картина
Като цяло, неоплазмите на мастните жлези, възникващи под нивото на шията, са по-силно свързани със синдром на Muir-Torre, отколкото тези, които възникват около окото или ухото. Измененията, които не са в областта на главата и шията, са по-често свързани с мутации в рецептора на епидермалния растежен фактор.
Кожните неоплазми (новообразувания), появяващи се по лицето, торса и крайниците, са срещат и при различни други заболявания, включително:
- синдром на Гарднър (Gardner syndrome)
- синдром на Коуден (Cowden syndrome)
- множествени трихоепителиоми
- базалноклетъчен невус синдром
- еруптивни кератоакантоми
- туберозна склероза
Голяма част от тези синдроми са също свързани и с висцерални тумори.
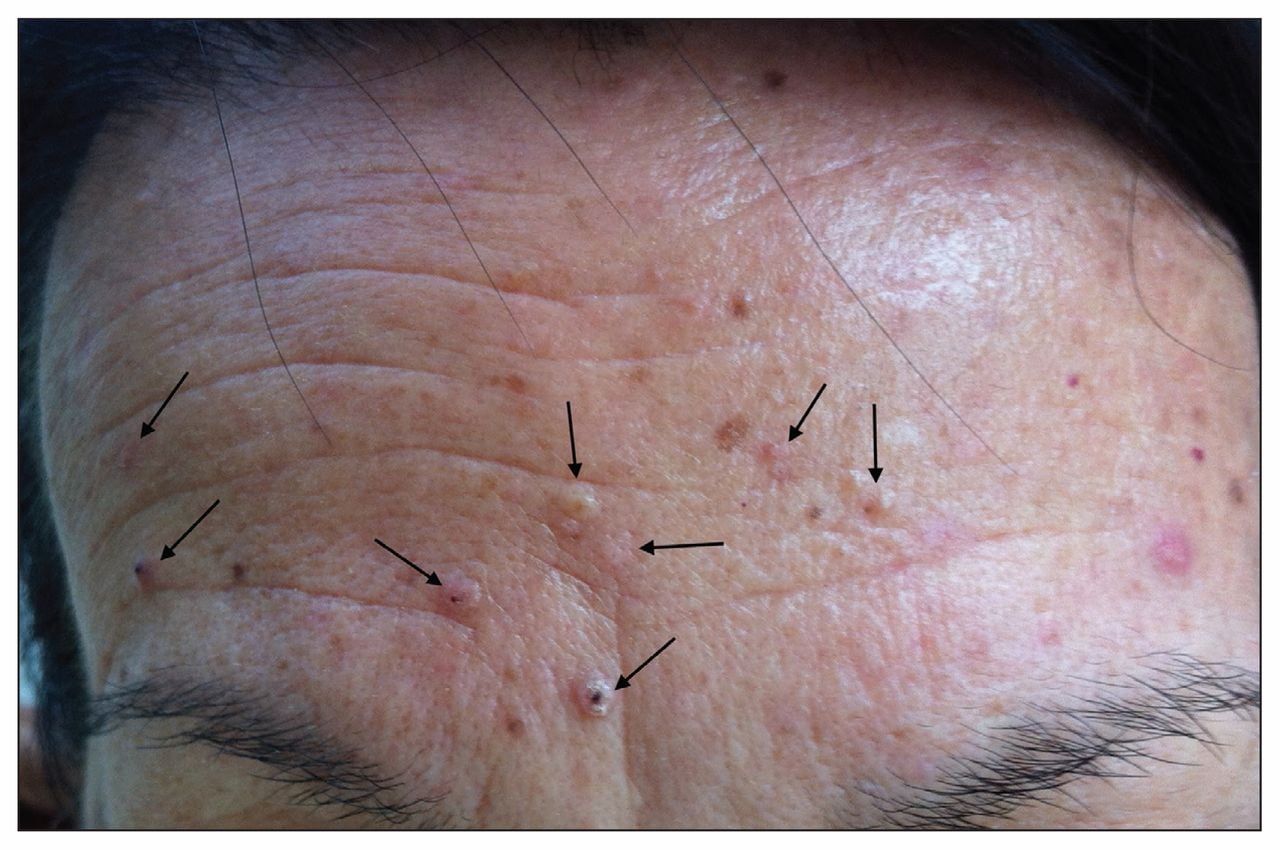
Изображение: www.cmaj.ca
Себацейният аденом е най-характерния маркер за синдрома на Muir-Torre. Този сравнително рядък, доброкачествен тумор обикновено се появява под формата на жълти папули (папула - малко, плътно и леко надигнато над нивото на кожата образувание, с големина до лещено зърно) или нодули (възелчета) при възрастни пациенти.
В епизодични случаи, повечето тумори са разположени върху главата (особено на лицето, скалпа и клепачите), а останалата малка част са разпръснати по останалата част на тялото.
Клиничните характеристики на себацейните епителиоми са сходни.
Себацейните карциноми се появяват най-често на клепачите, където те обикновено възникват от Мейбомиевата (meibomian) жлеза (мастна жлеза, намираща се в клепачния ръб) и жлезите на Цайс (Zeiss) - мастни жлези, намиращи се в основата на миглите на окото. Тези карциноми могат да се появят почти навсякъде по кожата, включително и по ушите, краката, пениса и срамните устни.
По клепачите туморът се появява като твърд, жълт възел, с тенденция за разязвяване. Клинично, тези лезии често се бъркат с халазия (кистичка на горен или долен клепач, причинена от възпаление на жлеза на клепача), хроничен блефароконюнктивит или карбункул. Себацейният карцином на очния клепач може да засегне очната кухина, като често метастазира.
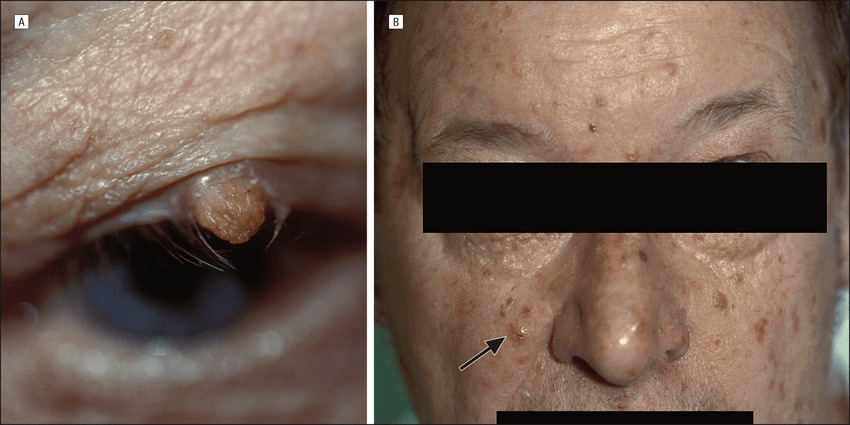
Изображение: www.researchgate.net
Разграничаването на себацеен карцином от аденом/епителиом обикновено се базира на архитектурата на лезията (инфилтративна при карцином и като окръжност при аденом/епителиом). Въпреки това, някои лезии заграждат граници, но показват чиста цитологична (клетъчна) атипия.
Кератоакантом, единичен или множествен, се наблюдава често при синдром на Muir-Torre. Обикновено започва като червена пъпчица, която бързо нараства и се превръща в лъскаво възелче, което е с цвета на околната кожа, с телеангиектазии и централно роговично поле, покрито с коричка.
Най-често засегнатите места са предната и задната повърхност на ръцете, но могат да се появят навсякъде по тялото. Туморите са с тенденция за обратно развитие, като оставят белег.
Съпътстващи новоообразувания
Най-често срещаното висцерално новообразувание при синдром на Мюр-Тор е колоректален карцином, появяващ се в почти половината от пациентите.
Второто най-често място за развитие е пикочо-половата система, като случаите включват около 1/4 от пациентите.
Съобщава се и за множество други видове рак, включително рак на гърдата, лимфом и рядко левкемия, тумори на слюнчените жлези, тумори на горните и долните дихателни пътища, а също и хондросарком.
Чревни полипи се появяват в поне 1/4 от пациентите.
Други доброкачествени тумори, описани при MTS, включват гранулозно-клетъчен тумор на яйчниците, чернодробна ангиома, доброкачествен шваном на тънките черва и лейомиоми на матката.
Диференциална диагноза
Диференциалната диагноза се прави с:
- базалноклетъчен карцином
- синдром на Гарднър
- кератоакантом
- себацеен аденом
- себацейна хиперплазия
- плоскоклетъчен карцином
- трихоепителиом
- туберозна склероза.
Диагноза
Критериите за диагностика на MTS включват присъствието на най-малко едно новообразувание, произхождащо от мастните жлези (себацеен аденом, епителиом, карцином, както и базалноклетъчен карцином със себацейна диференциация) и поне един висцерален карцином.
Около 40% от герминативните мутации (наследствени мутации) при наследствения неполипозен колоректален карцином са в hMSH2 (human mutS homolog 2) гена и около 35% са в hMLH1 (human mutL homolog 1) гена, докато при синдрома на Мюр-Тор по-голямата част от мутациите са в hMSH2 гена. Други маркери, които могат да бъдат изменени в някои от случаите, са MSH-6 (mutS homolog 6) и PMS-2 (postmeiotic segregation increased 2).
Тези мутации могат да бъдат открити чрез генетични изследвания на периферна кръв или чрез имунохистохимичен анализ (идентифициране на различни видове клетки чрез свързването на антитела към специфични части от клетката) на проба, получена при биопсия.
Наличие на гваякол (метоксифенол) в изпражненията може да бъде насочващо за откриването на карциноми на дебелото черво, но при евентуален MTS трябва да се извърши колоноскопия.
Микроскопско изследване
При клиничната диагноза на лезиите на мастните жлези може да се използват дерматоскопия и конфокален микроскоп (оптичен флуоресцентен микроскоп, притежаващ значително по-голям контраст от обикновения микроскоп).
Дерматоскопските характеристики включват:
- радиално разположени, завити като корона кръвоносни съдове, които обграждат непрозрачни и безструктурни жълти области или жълти комедоподобни (псевдофоликулни) глобули (малко сферично тяло)
- разклоняващи се кръвоносни съдове.
Конфокалната микроскопия разкрива себацейни лобули (делче, малък лоб), съставени от групи от овални клетки с тъмни ядра и ярка, лъскава цитоплазма. Тези клетъчни групи са разделени от линия от епителни клетки, които съответстват на базалоидни клетки.
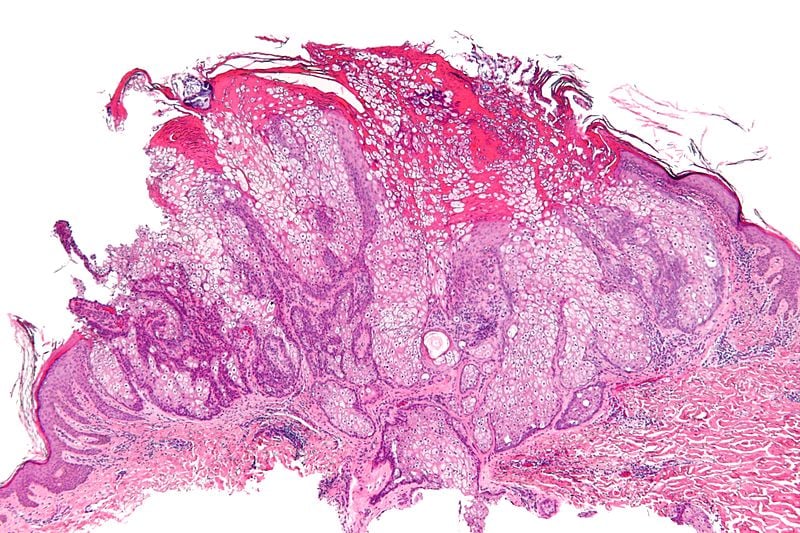
Изображение: Nephron, CC BY-SA 3.0, via Wikimedia Commons
Хистология
Аденомът на мастните жлези се състои от непълно диференцирани лобули с различен размер. Лобулите съдържат базалоидни клетки в периферията и зрели себацейни клетки, които са с характерни цитоплазмени вакуоли (вакуола - мехурче, което съдържа електролити, вода, въглехидрати и пигменти) около центъра.
Себацейният епителиом (познат и като себацеом - sebaceoma) се различава от себацейния аденом главно по отношение на степента на диференциране. При себацейните епителиоми липсва лобуларната архитектура и зреенето на мастните жлези, както е при себацейния аденом, и съдържа значителен процент недиференцирани клетки.
Себацейният карцином е злокачествено новообразувание със значителен клетъчен плеоморфизъм (способност на клетките да се проявяват в повече от една форма) и анаплазия (загуба на структурна диференциация на клетка или на група от клетки). Това заболяване се среща често на клепача и има склонност да се представи с пейджетоиден (клетките от долните слоеве на епидермиса се придвижват към горните епидермални слоеве) тип растеж на атипичните себацейни клетки в конюнктивата или в епидермиса. Понякога тумора засяга мастната тъкан на очницата (очната кухина).
Особено полезно при диагностиката на себацейния карцином е откриване на засегнат покриващ епител (на конюнктива или епидермис), подобно на болестта на Paget (Пейджет).
Кератоакантомът при синдрома на Muir-Torre често показва типичните хистологични (тъканни) характеристики на спорадичните (появяващи се от време на време) кератоакантоми - изразена епителна пролиферация (увеличаване на боря на клетките чрез размножаване) и хлътване, запълнено с голяма кератинова "запушалка".
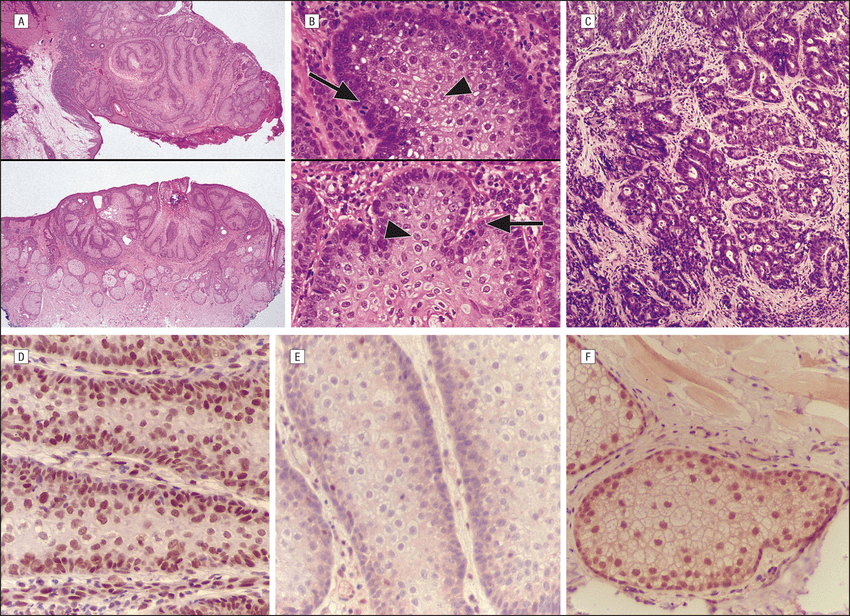
Изображение: www.researchgate.net
Имунохистохимия
Имунохистохимичното изследване може да бъде полезно в диференциалната диагноза на доброкачествени и злокачествени себацейни неоплазми.
При карциномите се наблюдава силна експресия на p53 (туморен протеин 53).
Имунохистохимичното доказване на загубата на hMSH2, hMSH6 и рядко на hMLH1 и PM2S гените е характерно за MTS и значително подсказва за герминативна мутация, която може да бъде потвърдена с допълнителни генетични тестове и консултации.
Липсата на тази находка не изключва синдром на Мюр-Тор, а скрининговата оценка за вътрешно злокачествено заболяване трябва да се има предвид при пациенти със себацейни неоплазми, различни от хиперплазия на мастните жлези.
Основната аномалия, открита при синдрома на Muir-Torre, е промяната в гените за репарация на неправилно сдвоени бази, особено MSH2 (MutS protein homolog 2) гена в хромозома 2 и MLH1 (MutL homolog 1) гена в хромозома 3. Другите гени са MSH-6, MLH-3 и PMS-2. При себацейния карцином се наблюдава загуба на два от ретиноидните рецептори (RXR-бета и RXR-гама).
Лечение
Лечението включва орален (през устата) прием на изотретиноин (isotretinoin), който вероятно може да предотврати някои от неоплазмите при хора със синдром на Muir-Torre.
Доброкачествените тумори и кератоакантомите на мастните жлези могат да бъдат лекувани консервативно с ексцизия (изрязване) или криотерапия.
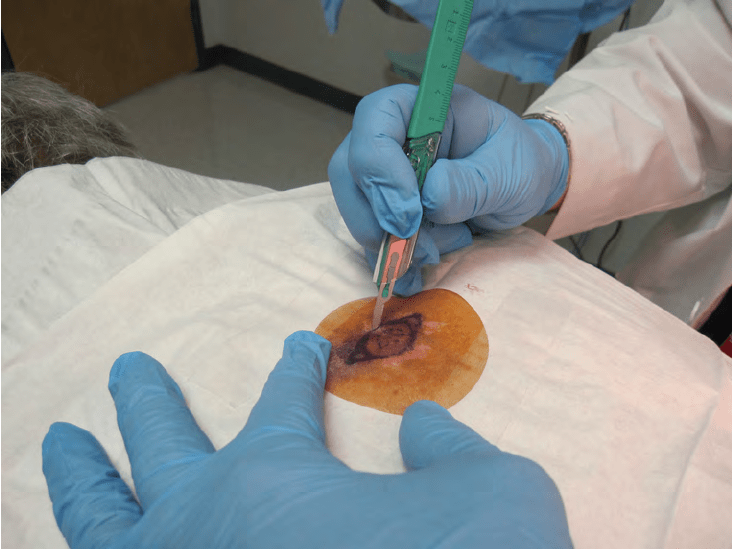
Изображение: www.researchgate.net
Профилактика
Пациентите със синдром на Muir-Torre (MTS) трябва да си провеждат редовно пълни прегледи, особено на стомашно-чревния тракт и пикочо-половите пътища.
Годишна колоноскопия след навършване на 25 години е желателна, като причината е високата честота на проксимален колоректален рак.
Проследяването на пациентите при рецидив или метастази е задължително.
Роднините на пациентите трябва да получат генетична консултация.
Миелопролиферативни неоплазми
Включените в МКБ D09.7 Карцином in situ с други уточнени локализации представляват хетерогенна (разнородна) група от заболявания, характеризиращи се с клетъчна пролиферация (увеличаване на броя на клетките чрез размножаване) на една или повече хематологични (свързани с кръвта) клетъчни линии в периферната кръв, различни от остра левкемия.
Класификация
Според френско-американско-британската (French-American-British - FAB) класификация хроничните миелопролиферативни неоплазми се състоят от четири заболявания:
- хронична миелогенна левкемия (ХМЛ);
- полицитемия вера (ПВ);
- есенциална тромбоцитемия (ЕТ)
- идиопатична миелоидна метаплазия (ИММ), която е известна и като миелофиброза.
През 2002 година Световната здравна организация (СЗО) предлага алтернативна схема за класификация на тези заболявания, като добавя хронична неутрофилна левкемия (ХНЛ) и хронична еозинофилна левкемия (ХЕЛ)/хипереозинофилен синдром (ХЕС).
Подобно заболяване е системната мастоцитоза (СМ), която има много общи черти с миелопролиферативните заболявания и според някои автори принадлежи към тази група от заболявания.
Миелопролиферативно заболяване може да се трансформира в друго миелопролиферативно новообразувание, да се развие до остра левкемия или и двете.
Патогенеза
Някои данни показват, че миелопролиферативните неоплазми възникват от злокачествена трансформация на единична стволова клетка. В хроничната фаза на хроничната миелогенна левкемия се ангажират еритропоезата, неутрофилопоезата (процес на образуване на неутрофили), еозинофилопоезата (процес на образуване на еозинофили), базофилопоезата (процес на образуване на базофили), моноцитопоезата (процес на образуване на моноцити) и тромбоцитопоезата (процес, при който се образуват тромбоцити).
Данните от различни изследвания са установили, че миелопролиферативните заболявания имат клонален произход, а обща характеристика на тези нарушения се явява придобитата активираща мутация в гена, кодиращ различни тирозин-кинази.
Тирозин-киназната активност на BCR-ABL (breakpoint cluster region-Abelson murine leukemia viral oncogene homolog 1) хибридния ген се увеличава при хроничната миелогенна левкемия. Преобладаващата генетична лезия при полицитемия вера, есенциална тромбоцитемия и миелофиброза е заместване на валин за фенилаланин на позиция 617 (V617F) в Janus киназния ген 2 (JAK2), което води до свръхчувствителност към еритропоетин.
Системната мастоцитоза е свързана с D816 мутация в KIT (v-kit Hardy-Zuckerman 4 feline sarcoma viral oncogene homolog) гена, а FIP1L1-PDGFR мутацията е установена в подгрупа от пациенти със системна мастоцитоза (натрупване на мастоцити) и еозинофилия (повишено количество на еозинофили в кръвта) - SM-EOS.
Епидемиология
Честотата на разпространение на полицитемия вера е 0.02-2.8 на 100 000 човека, като в Япония е с най-ниска честота. Есенциалната тромбоцитемия се среща в 0.1-1.5 на 100 000, миелофриброзата - 0.4-0.9 на 100 000.
Най-често са засегнати индивидите между 40 и 60-годишна възраст, като появата на миелопролиферативни заболявания е необичайно при хора, които са по-млади от 20 години.
Етиология
Както и при други злокачествени заболявания, точната причина за развитието на миелопролиферативните неоплазми е неизвестна. Етиологията е сложна, не напълно изяснена и вероятно е многоетапен процес, който включва повече от един ген.
При повечето пациенти, които имат хронична миелогенна левкемия, се установява Филаделфийска хромозома - транслокация на хромозоми 9 и 22, t(9:22). Дори когато липсва Филаделфийска хромозома, генът bcr-abl, образуван в резултата на t(9:22), се позитивира при тестване на пациенти с хронична миелогенна левкемия. Генът bcr-abl кодира хибриден протеин с тирозин-киназна активност, който се експресира и се разглежда като централен механизъм, който е в основата на хроничната фаза на хроничната миелогенна левкемия.
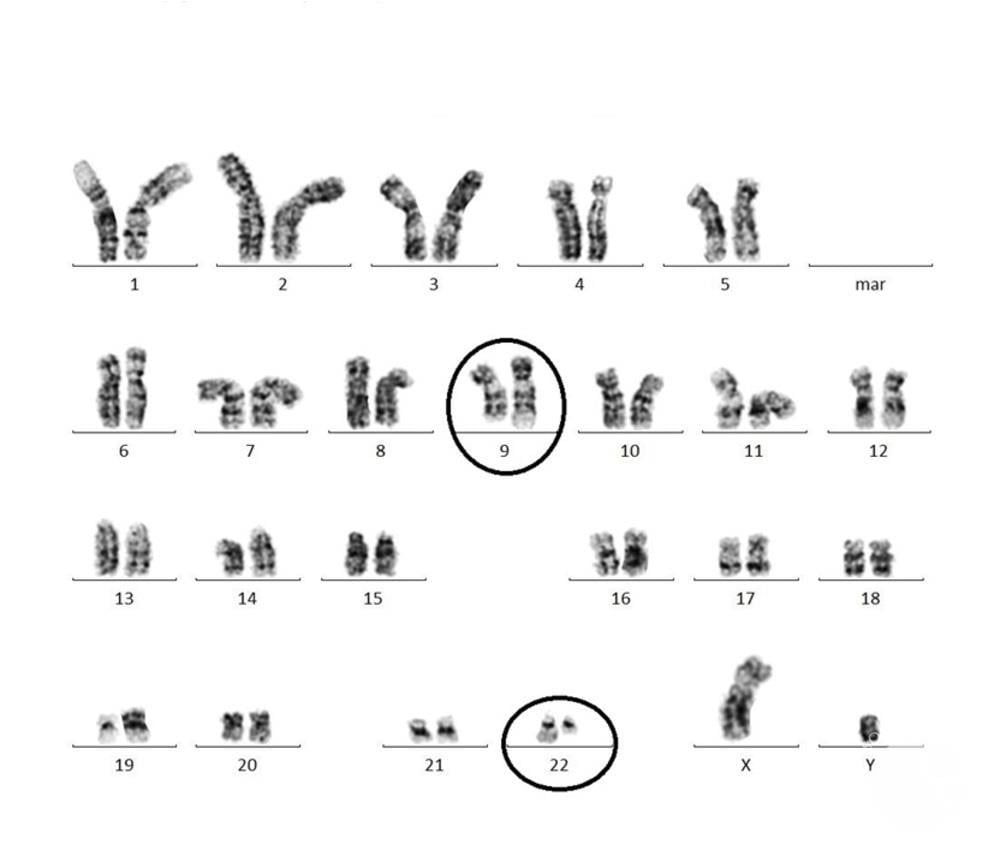
Изображение: hematology.org
Клинична картина
Клиничните прояви включват лесна уморяемост, анорексия, загуба на тегло. Коремен дискомфорт и ранно засищане при спленомегалия (увеличени размери на слезката (далака) се срещат по-често при хронична миелогенна левкемия и идиопатична миелоидна метаплазия.
Други прояви са лесната поява на синини, кървене и/или симптоми на тромбоза, подути и болезнени стави като вторична изява на хипеурикемия (увеличени нива на пикочната киселина или урати в кръвта).
При левкостаза (означава се и като симптоматична хиперлевкоцитоза - левкоцитите са над 100 х 109/l) се наблюдава приапизъм (постоянна ерекция, дори без стимул), тинитус (шум в ушите) или ступор (състояние на обездвижване без загуба на съзнание).
Болки в горен ляв квадрант на корема и в лявото рамо се наблюдават като последствие от инфаркт на слезката и периспленит (възпаление на перитонеалната повърхност на далака).
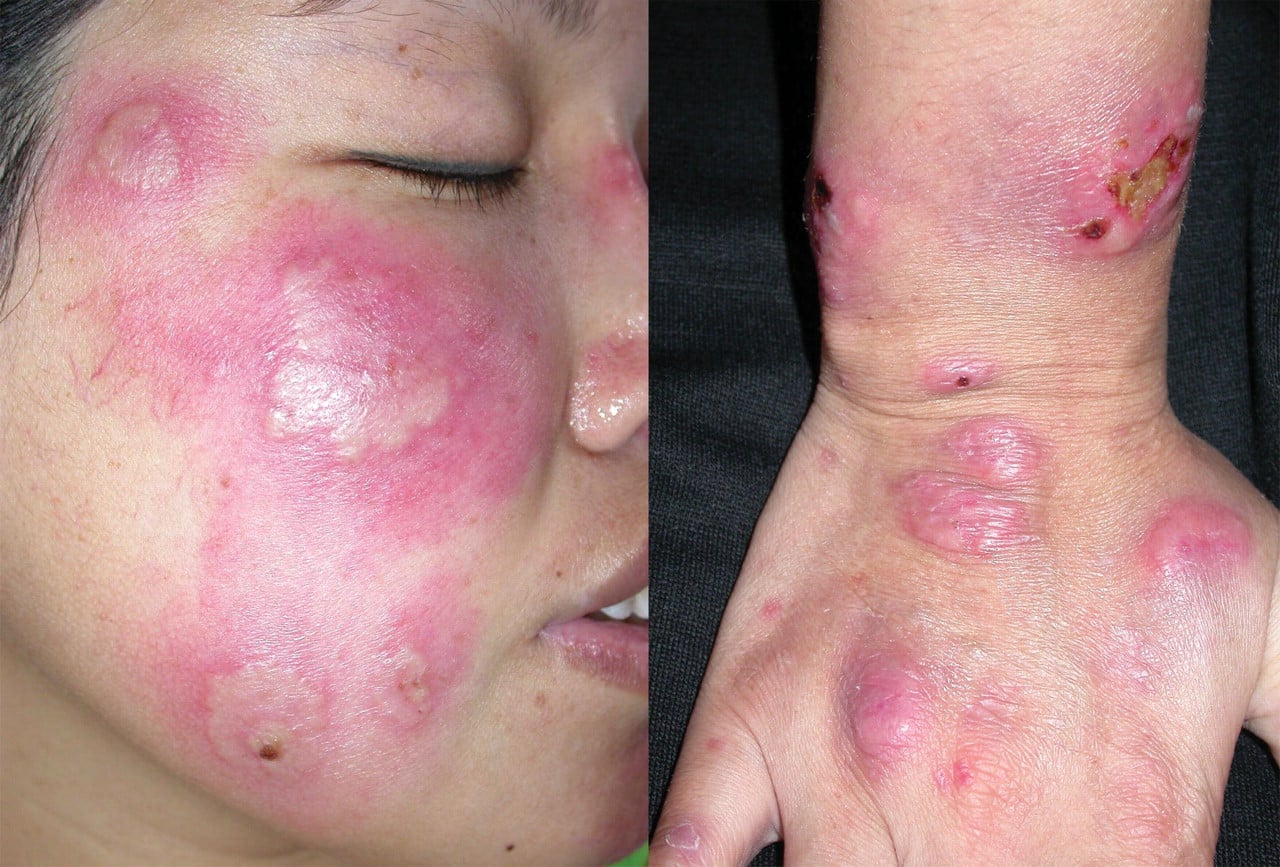
Изображение: Sweet syndrome/www.cmaj.ca
При физикалното изследване се установяват избледняване на кожата и видимите лигавици, освен при пациенти с полицитемия вера; плетора (пълнокръвие - увеличен общ обем на кръвта) при полицитемия; петехии и екхимози - различни по големина кръвоизливи; увеличени далак и/или черен дроб.
Понякога се наблюдава синдром на треска, придружен от болезнени макуло-папулозни (вид обривни елементи) виолетови лезии по торса, ръцете и лицето, което се означава като остра фебрилна неутрофилна дерматоза или синдром на Sweet.
Диагноза
Диагнозата на тези заболявания се поставя с различни клинични и лабораторни методи:
Лабораторни изследвания
- пълна кръвна картина и диференциално броене с микроскопско изследване на натривка от периферна кръв;
- изследване на алкалната фосфатаза в левкоцитите (АФ, alkaline phosphatase - ALP) - спомага за диференциране на хронична миелогенна левкемия от други причини за левкоцитоза;
- полимеразна верижна реакция (Polymerase Chain Reaction, PCR) или флуоресцентна ин ситу хибридизация (fluorescence in-situ hybridization, FISH) - могат да открият прегрупиране на bcr-abl гена и така се прави разграничаване на хронична миелогенна левкемия от други миелопролиферативни заболявания;
- изследване на еритроцитен концентрат (еритроцитна маса);
- определяне на серумните нива на пикочната киселина;
Образна диагностика
Въпреки че не се прави рутинно, изследването на черния дроб и далака с компютърен томограф (КТ) понякога може да бъде полезно, за да се оцени размера на тези органи при диагностицирането на заплетени случаи;
Други тестове
Молекулярни тестове за откриване на bcr-abl ген, когато се подозира хронична миелогенна левкемия и при отрицателни тестове за Филаделфийска хромозома;
PCR изследване на костния мозък за JAK2 гена е възможно при съмнения за полицитемия вера, есенциална тромбоцитемия или миелофиброза.
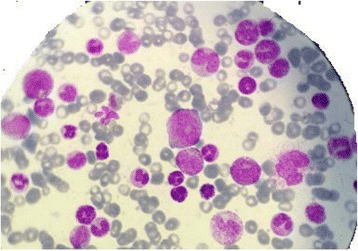
Изображение: Elm'hadi C1,2, Khmamouche MR3, Tanz R3, Toreis M3, Mahtat E4, Allaoui M5, Oukabli M5, Messaoudi N6, Errihani H7, Ichou M3., CC BY 4.0, via Wikimedia Commons
Процедури
Аспирация и биопсия на костен мозък с цитогенетични проучвания са необходими при повечето, но не при всички пациенти. Цитогенетичните изследвания откриват наличие или отсъствие на Филаделфийска хромозома и помагат за разграничаването на тези нарушения от миелодиспластичен синдром.
Диференциална диагноза
Диференциалната диагноза при миелопролиферативните заболявания се прави с:
- остра лимфобластна левкемия;
- остра миелогенна левкемия;
- идиопатична миелоидна метаплазия с миелофиброза;
- хронична лимфоцитна левкемия;
- хронична миелогенна левкемия;
- хипереозинофилен синдром;
- неходжкинов лимфом;
- системна мастоцитоза;
- спленомегалия;
- есенциална тромбоцитоза;
- вторична тромбоцитоза;
- хипергамаглобулинемия на Waldenstrom;
Лечение
Хроничната миелогенна левкемия (ХМЛ)
Лечението на хроничната миелогенна левкемия (ХМЛ) включва:
- трансплантация на хематопоетични стволови клетки при млади пациенти в хроничната фаза на заболяването, ако е налице подходящ донор с HLA (human leukocyte antigen)-съвместимост;
- приложение на иматиниб мезилат - bcr-abl-специфичен инхибитор на тирозин-киназата
- интерферон алфа - води до хематологични и молекулярни ремисии при някои пациенти, като по този начин удължава преживяемостта;
Чрез добавянето на ниски дози цитозин арабинозид към интерферон алфа се постигат по-високи нива на ремисия. Пациенти, които имат непоносимост към терапията с интерферон алфа, могат да бъдат лекувани с хидроксиурея (hydroxyurea) .
- дазатиниб (dasatinib) е показан за лечение на възрастни пациенти с ХМЛ в хронична, ускорена, миелоидна или лимфоидна бластна фаза, които са резистентни или имат непоносимост към предишна терапия, включваща иматиниб;
- нилотиниб (nilotinib) - киназен инхибитор, който е показан за лечение на хронична и ускорена фаза на положителна за Филаделфийска хромозома хронична миелогенна левкемия при възрастни пациенти, които са резистентни или с непоносимост към предишното лечение, включващо иматиниб;
Когато заболяването прогресира до бластна фаза, то се третира като остра левкемия;

Изображение: www.freepik.com
Есенциалната тромбоцитемия (ЕТ)
Лечението на есенциалната тромбоцитемия (ЕТ) е насочено към облекчаване на симптомите и предотвратяване на усложненията. Целта на лечението е да се запази броят на тромбоцитите в референтни граници, а това обикновено се постига чрез прилагане на хидроксиурея (hydroxyurea) и анагрелид (anagrelide).
Миелофиброза (МФ)
За момента няма достъпно лечебно средство за лечение на миелофиброза (МФ). Асимптоматичните пациенти могат да бъдат наблюдавани клинично до поява на симптоми. Хидроксиуреята е подходяща за потискане на броя на циркулиращите клетки.
Пациенти с болезнени, значително увеличени далаци, които не се поддават на миелосупресивна терапия, понякога се подлагат на лъчева терапия, но в крайна сметка могат да изискват спленектомия (хирургично премахване на далака).
Медикаментите, които се прилагат при миелопролиферативните неоплазми, имат за цел да ограничат заболеваемостта и да предотвратят усложнения. Използват се различни групи лекарства:
- интерферони (интерферон алфа-2а и интерферон алфа-2б) - това са естествено произвеждани протеини с антивирусни, антитуморни и имуномодулиращи (имуностимулиращи) действия. Интерфероните могат да бъдат приложени локално, системно и в лезията;
- антиметаболитни препарати - инхибират (потискат) клетъчния растеж и пролиферация (размножаване). Такива лекарства са: хидроксиурея (hydroxyurea); анагрелид (anagrelide); руксолитиниб (ruxolitinib);
- тирозин-киназни инхибитори - тези вещества инхибират активността на bcr-abl тирозин-киназата, което води до намалена пролиферация и повишена апоптоза (програмирана клетъчна смърт) в клетъчни линии, позитивни за Филаделфийска хромозома. Към тези лекарства се отнасят: иматиниб мезилат (imatinib mesylate); дазатиниб (dasatinib); нилотиниб (nilotinib);
Понякога мерките при тези заболявания включват спленектомия за симптоматично облекчаване на болката, свързана със значителна спленомегалия - увеличени размери на далака (слезката), неподатлива на медикаментозно лечение.
На пациентите с миелопролиферативни заболявания, при които няма нужда от ограничаване на техните ежедневни дейности, се препоръчва да се въздържат от тежка физическа активност, защото има опасност от коремна травма, тъй като значително уголемените далаци са склонни към руптура (разкъсване), понякога дори и при минимална травма.
Заглавно изображение: www.freepik.com
Коментари към Карцином in situ с други уточнени локализации МКБ D09.7