Карцином in situ на хранопровод МКБ D00.1
В това МКБ D00.1 Карцином in situ на хранопровод се включват двете най-често срещани преканцерозни (предракови) състояния на хранопровода — плоскоклетъчен карцином in situ и аденокарцином in situ.
Хранопроводът — oesophagus (esophagus), е тясно и дълго тръбесто образувание, което провежда храната и течностите от гълтача до стомаха. Дължината му достига 25-30 см. На хранопровода се различават три части — шийна, гръдна и коремна. Лигавицата на хранопровода се покрита от многослоен плосък епител, който е изграден от 20-24 слоя. Плоските клетки от повърхностните слоеве съдържат в цитоплазмата си отделни кератохиалинни зърна, без обаче да вроговяват. Собствената пластинка — lamina propria (ламина проприя), се изгражда от колагенни и еластични влакна, между които се намират множество лимфоцити и лимфни фоликули. Под лигавицата се разполага добре развит подлигавичен слой — tela submucosa, изграден от колагенни и еластични влакна. Лигавицата и подлигавичния слой на хранопровода са устроени така, че позволяват значително стеснение и разширение на неговия просвет.
Повече за анатомичното устройство на хранопровод може да прочетете при:
Първичните тумори на хранопровода се класифицират като епителни и неепителни в зависимост от клетъчния произход и могат да бъдат доброкачествени или злокачествени. Неепителните тумори произлизат от мезенхимна или стромална (строма — опорна структура на даден орган) тъкан.
Предраковите изменения не се срещат при всички първични ракови заболявания на хранопровода.
В световен мащаб, плоскоклетъчния карцином е най-често срещания рак на хранопровода, докато в западните страни преобладават случаите с аденокарциноми.
Прогнозата и при двата вида рак е лоша, като причина за това е, че симптомите се проявяват, когато вече туморите са прогресирали.
Ранното откриване и лечение подобрява прогнозата, поради което е необходимо да се установи и разбере патологията на премалигнените (предраковите) лезии. По този начин е възможно състоянията, които са с висок риск за злокачествена прогресия, да бъдат идентифицирани и лекувани в много по-ранен етап.
Сквамозноклетъчният (плоскоклетъчен) карцином (SCC) на хранопровода е злокачествен епителен тумор с плоскоклетъчна диференциация, с видими под микроскоп кератиноцитоподобни клетки и междуклетъчни мостчета и/или кератинизация.
SCC на хранопровода показва голямо географско разнообразие в заболеваемостта, смъртността и съотношението между половете. Този вид рак е много по-често срещан в страните от Източна Европа и в много от развиващите се страни.
Рискови фактори
В западните страни най-значителните рискови фактори за развитие на плоскоклетъчен карцином са тютюнопушенето и алкохола, като всеки от тези фактори повишава риска от рак на хранопровода по различен начин.
По отношение употребата на тютюн, умереният прием през дълъг период от време носи по-висок риск в сравнение със значителен прием за кратък интервал от време, докато обратната зависимост е характерна за алкохола.
Комбинирани, двата фактора показват значително по-силен ефект, дори при нисък прием на алкохол.
Полиморфизъм (наличие на повече от една форма) в ALDH2 (Aldehyde dehydrogenase 2 family (mitochondrial)), генът, кодиращ алдехид дехидрогеназа 2, значително увеличава риска за развитие на ракови заболявания на горния храносмилателен тракт, включително плоскоклетъчен карцином. Това предполага роля на ацеталдехида, един от основните канцерогенни метаболити на алкохола, в развитието на карцином на хранопровода.
Съществуват и други фактори, освен тютюн и алкохол, които играят значителна роля в развитието на този карцином:
- някои храни;
- топли напитки — това е един от най-често срещаните рискови фактори, водещ до хроничен езофагит и след това до преканцерозно заболяване;
- инфекции с човешки папилома вирус (HPV);
- други — ахалазия, синдром на Плъмър-Винсън (Plummer-Vinson), цьолиакия и тилоза (фокална неепидермолитична палмоплантарна кератодермия)
Подробна информация за злокачествените заболявания на хранопровода ще намерите при:
Плоскоклетъчен карцином in situ на хранопровода:
Развитието на плоскоклетъчен карцином in situ на хранопровода се смята за многоетапен процес, който започва с превръщането на нормалния плосък епител до такъв с базалноклетъчна хиперплазия (хиперплазия - увеличаване на броя на клетките), последваща интраепителна неоплазия (дисплазия и карцином in situ) и накрая — инвазивен SCC.
За да се изгладят различията в диагностичните критерии при "реактивни промени", "нискостепенна дисплазия" и "високостепенна дисплазия", е създадена нова класификация за епителна неоплазия по време на Световния конгрес по гастроентерология, проведен през 1998 във Виена. На тази среща е решено диагнозите "високостепенна дисплазия" и "неинвазивен карцином (карцином in situ)" се сливат в по-общата "неинвазивна високостепенна дисплазия". От своя страна, Световната здравна организация (СЗО) променя термина "дисплазия" в "интраепителна неоплазия".
Интраепителната неоплазия се среща около осем пъти по-често във високорисковите райони и често се наблюдава в непосредствена близост до инвазивен плоскоклетъчен карцином — в тъканни проби, получени при езофагектомия (хирургично отстраняване на хранопровода).
Патоморфология
Морфологичните особености на интраепителната неоплазия включват както структурни, така и цитологични (клетъчни) аномалии. Структурните особености се характеризират с дезорганизация на епитела и загуба на нормалната клетъчна полярност.
Цитологично, клетките се характеризират с:
- неправилни и хиперхромни (по-силно оцветени) ядра;
- увеличено съотношение ядро: цитоплазма;
- висока митотична (митоза — вид клетъчно делене) активност.
Плоскоклетъчната епителна дисплазия (неоплазия) е преканцерозната лезия, от която се развива плоскоклетъчен карцином и при която хистологично се наблюдават атипични сквамозни (плоски) клетки, при които е нарушена нормалната сквамозна диференциация, която трябва да се наблюдава между базалните (намиращите се в основата) и повърхностните клетки. Ако не се наблюдава никаква диференциация и повърхностните клетки изглеждат като базалните епителни клетки, то тази промяна се означава като плоскоклетъчен карцином in situ.
Дисплазията обикновено се класифицира като ниско- или високостепенна.
При нискостепенната аномалиите най-често са ограничени до по-малко от долната половина на базалния слой на епитела, докато при високостепенната дисплазия анормални клетки се появяват и в горната половина на епитела и показват по-голяма ниво на атипизъм, а освен това при този тип дисплазия липсва зреене и клетъчната атипия заема повече от половината дебелина на епитела.
При карцином in situ атипични клетки се наблюдават през дебелината на целия епител, без доказателства за тяхното зреене на повърхността на епитела.
Ако степента на дисплазия се промени от лека през умерена до тежка (високостепенна), значително се увеличава и рискът за развитие на плоскоклетъчни новообразувания в хранопровода.
Плоскоклетъчната дисплазия като цяло се визуализира при ендоскопия, особено ако хранопроводът е третиран с йодин.
Епидемиологични проследяващи проучвания показват повишен риск за последващо развитие на: инвазивен SCC при пациенти с базоцелуларна (базалноклетъчна) хиперплазия (относителен риск (ОР): 2.1); ниска степен на дисплазия (ОР: 2.2); умерена дисплазия (ОР: 15.8); високостепенна дисплазия (ОР: 72.6) и карцином in situ (ОР: 62.5).
Базалноклетъчната хиперплазия хистологично се определя като иначе нормален плоскоклетъчен епител, с дебелина на базалната зона, която е по-голяма от 15% от общата дебелина на епитела, без да е налице удължаване на папилите (пръстовидни израстъци) на lamina propria. В повечето случаи базалноклетъчната хиперплазия представлява епителна пролиферативна лезия, която се развива като отговор при езофагит — често наблюдавано при високорискови за рак на хранопровода популации.
Друго прекурсорно заболяване при плоскоклетъчния карцином на хранопровода е плоскоклетъчният папилом. Това е рядко срещано заболяване и не причинява специфични симптоми, като обикновено се открива случайно при ендоскопия. Представлява доброкачествен тумор, с по-малко от 200 случая, съобщени в литературата и съставен от хиперпластичен плоскоклетъчен епител, покриващ пръстовидни израстъци, имащи сърцевина, произхождаща от lamina propria. Тези израстъци са гладки, добре оформени и с диаметър 5 мм или по-малко.
Много рядко се срещат и гигантски папиломи с размери до 5 см.
Етиология
Хронично възпаление на лигавицата и инфекция с човешки папилома вирус (HPV) са двете възможни етиологични причини. Въпреки това, точната причина за развитие на сквамозноклетъчен папилом на хранопровода е неизвестна, а злокачествена прогресия до SCC е изключително рядко явление, като за някои автори е спорно и дали това състояние може да доведе до развитие на рак на хранопровода.
Плоскоклетъчните папиломи обикновено се развиват при възрастни и се срещат при 0.01% до 0.4% от индивидите (много рядко се срещат и при деца), като повечето (85%) сквамозноклетъчни папиломи представляват солитарни (единични) изолирани лезии, които обикновено са разположени в дисталната (далечната) и средната трета на хранопровода, въпреки че при някои пациенти се срещат и множествени папиломи. Наличието на ендоскопски диагностициран папилом на хранопровода се съобщава само в няколко случаи, като честотата му варира от 0.01% до 0,43%.
Сквамозните папиломи се виждат като мънички полипи при ендоскопия, а по лигавицата при биопсичните проби се виждат белезникави възелчета. Микроскопски, тези лезии са съставени само от тънка плоскоклетъчна лигавица с фиброваскуларни структура.
Циркумферентен (циркулярен) плоскоклетъчен папилом в шийната част на хранопровода представлява изключително рядка причина за дисфагия, но е описано успешното лечение на такъв случай с локално приложение на S-1-цитокин.
В такива случаи ендоскопската резекция (изрязване) трябва да се извършва заедно с прецизно хистологично (тъканно) изследване (включително полимеразна верижна реакция (PCR) за HPV вирус) на отстранената тъкан.
Вторият вид карцином in situ, който е разгледан в МКБ D00.1 Карцином in situ на хранопровод, е:
Аденокарцином in situ на хранопровода:
Това новообразувание представлява злокачествен епителен тумор на хранопровода, с жлезна диференциация, произтичаща предимно от Баретова лигавица в долната трета на хранопровода. Рядко, аденокарциномът произхожда от хетеротопична (намираща се на различно от нормалното си местоположение) стомашна лигавица в горната част на хранопровода или от жлези, намиращи се в лигавицата и подлигавицата.
Честота
Честотата и разпространението на аденокарцинома на хранопровода в развитите страни са се повишили значително. Няколко проучвания в САЩ и няколко европейски страни показват, че честотата на езофагеален аденокарцином се е удвоила между началото на 70-те и края на 80-те години и продължава да се увеличава с 5%-10% годишно. Това се съпътства от повишена честота на аденокарциномите в областта на кардията (мястото, където хранопроводът се отваря в стомаха), както и от субкардиални (под областта на кардията) стомашни карциноми.
В допълнение към повишената заболеваемост, аденокарциномите на хранопровода и на гастроезофагеалната зона (зоната на свързване между хранопровода и стомаха) имат някои общи епидемиологични характеристики, които ясно ги отличават от плоскоклетъчния карцином на хранопровода и аденокарцинома на дисталните (по-далече разположените) стомашни части. Тези характеристики включват:
- висок превес на мъжкия пол (съотношение мъже: жени 7:1);
- по-висока честота сред бялата раса;
- средна възраст по време на диагнозата около 65 години;
Етиология
Съществуват няколко етиологични причини (причини за възникване) за развитието на неопластичен процес в хранопровода:
- епидемиологичните характеристики на аденокарцинома на дисталния хранопровод и на гастроезофагеалната връзка съответстват на тези, наблюдавани при пациенти с позната чревна метаплазия (способност на някои тъкани да се превръщат в друг вид тъкани, сходни на изходните) в дисталния хранопровод, т.е. Баретов хранопровод (Barrett's oesophagus), който е идентифициран като най-важната прекурсорна лезия и рисков фактор за аденокарцином на дисталния хранопровод, независимо от дължината на сегмента с чревна метаплазия;
- тютюнопушене - посочено като друг основен рисков фактор за езофагеален аденокарцином in situ;
- затлъстяване — също свързано с повишен риск за развитие на карцином, особено за лица с индекс на телесната маса (BMI) над 30;
- алкохол — за разлика от плоскоклетъчния карцином на хранопровода, при езофагеалния аденокарцином няма значителна връзка между неговото развитие и консумацията на алкохол;
- инфекция с Helicobacter pylori — тази инфекция не изглежда да бъде предразполагащ фактор за развитието на чревна метаплазия и аденокарцином в дисталната част на хранопровода. Според последните изследвания, инфектирането на стомаха с H. pylori може дори да има защитен ефект;
- дължината на хранопроводния сегмент с чревна метаплазия, както и присъствието на язви и стриктури (стеснения), са посочени като допълнителни рискови фактори за развитие на аденокарцином на хранопровода от някои автори;
Чревна метаплазия на хранопровода се развива, когато нормалния плоскоклетъчен епител на хранопровода се заменя от цилиндричен такъв по време на възстановителния период след повтарящи се наранявания на лигавицата на хранопровода, свързани обикновено с гастроезофагеална рефлуксна болест (ГЕРБ).
Чревна метаплазия може да бъде открита в повече от 80% от пациентите с аденокарцином на дисталния хранопровод.
Хроничният гастроезофагеален рефлукс е обичайната и основна причина за повтарящо се мукозно (лигавично) увреждане, а също така предоставя и анормална среда по време на лечебния процес, която предразполага към чревна метаплазия. Колкото по-чести, по-тежки и по-дълготрайни са симптомите на рефлукс, толкова е по-голям риска за развитие на аденокарцином. Рискът за развитие на аденокарцином при хора с дългогодишни и тежки симптоми на рефлукс е 43.5%. Въз основа на тези данни е постулирана причинно-следствена връзка между гастроезофагеален рефлукс (едно от най-често срещаните доброкачествени заболявания на храносмилателния тракт) и езофагеален аденокарцином.
Експериментални и клинични данни показват, че комбинираната експозиция (подлагане) на хранопровода на въздействието на стомашната киселина и дуоденалното (от дванадесетопръстника) съдържимо (жлъчни киселини и панкреатични ензими) има по-увреждащо въздействие, отколкото самостоятелното действие на стомашния сок или дуоденалното съдържание.
Комбинираният рефлукс увеличава риска за развитие на рак чрез стимулиране на клетъчната пролиферация (увеличаване на броя на клетките), както и чрез излагане на езофагеалния епител на потенциалното генотоксично (увреждащо генетичната информация в клетката, което причинява мутации, които могат да доведат до рак) стомашно и чревно съдържание, например нитрозамини.
Предразполагащите фактори за развитието на Баретов хранопровод и последващ аденокарцином при пациенти с гастроезофагеална рефлуксна болест включват значително удълженото време на въздействие на стомашното и дуоденалното съдържимо върху езофагеалната лигавица при рефлукс, като причината за това е нарушената бариерна функция на долния езофагеален сфинктер (ДЕС), както и неефективен клирънс (очистване) от страна на хранопровода.
Аденокарцином in situ на хранопровода може да се развие във всеки един сегмент на хранопровода, "облицован" с метапластична лигавица, съдържаща цилиндрични клетки (Баретов хранопровод), но най-често възникват в долната трета на хранопровода, в границите на сегмент с Баретов епител. В непосредствена близост до тумора може да се види типичната бледорозова лигавица на Баретовия хранопровод, особено при ранните карциноми. Характерните особености при аденокарцином, възникващ от Баретов хранопровод, в началото могат да приличат на неравности на лигавицата или на малки плаки. Повечето аденокарциноми, произхождащи от Баретов епител, са добре или умерено диференцирани и се характеризират с добре оформени тубуларни или папиларни структури.
Като изключение, аденокарцином in situ може да се развие също и в средната или проксималната трета на хранопровода, като това обикновено се дължи на вродени островчета от хетеротопичен цилиндричен епител (който присъства в до 10% от населението).
Патоморфология
Около 10% от пациентите с езофагит ще развият Баретова метаплазия, от които около 24% ще прогресират до дисплазия (промяна в клетъчния или тъканния вид).
Стадирането на дисплазията при хранопровод на Barrett се основава на четири основни характеристики на лигавицата при това заболяване, но с допълнителни хистологични характеристики, насочени към подпомагане разграничаването между дисплазия с неопределена значимост (IND), нискостепенна дисплазия (LGD) и високостепенна дисплазия (HGD).
Четирите основни характеристики включват:
- зреене на повърхностния епител вместо на подлежащите жлези;
- структура на жлезите при биопсия;
- цитологични (клетъчни) характеристики на пролифериращите (размножаващите се) клетки;
- възпаление и ерозии (увреждане на повърхностния слой на епитела)/язви;
Всяка от тези особености може да се изменя, както и могат да се съчетават, за да се стигне до диагноза.
При дисплазията с неопределена значимост (IND) може да се наблюдава нормална архитектура (структура) или определена степен на струпване на жлезите. При цитологичната оценка лезиите могат да са с:
- хиперхромазия (по-интензивно оцветяване);
- нарушения в ядрената мембрана;
- увеличен брой митози (вид клетъчно делене) в по-дълбоките слоеве;
- загубата на ядрена полярност не е характерна черта за IND;
Характеристика, която подпомага разграничаването на IND от нискостепенна дисплазия, е наличието на рязко "клонално" разграничаване на епителните промени.
Наличието на повърхностно зреене е полезна характеристика при отграничаване на потенциално реактивни лезии от наистина неопластични (диспластични) такива, като някои диспластични лезии демонстрират повърхностно зреене.
Нискостепенна дисплазия (LGD) може да се развие при около 18% от пациентите с над 1.5 — 4.3-годишно проследяване. Съществуват доказателства, че LGD може да остане неактивна в рамките на 57 месеца, преди да започне да прогресира.
При Баретов хранопровод с нискостепенна дисплазия повърхността изглежда подобна на подлежащите жлези при ниско увеличение на микроскопа или показва само леко узряване.
Структурата може да бъде леко до значително нарушена, със струпване на жлези, въпреки че lamina propria трябва да може да се разграничи между жлезите. Наблюдава се ядрена хиперхромазия с частично хроматиново струпване. Ядрата демонстрират нарушения в ядрената мембрана, но не са уголемени. При нискостепенната дисплазия нуклеолите (ядърцата) не са видими. Загуба на ядрена полярност също не е характерна за този вид дисплазия, въпреки че ядрена стратификация (разслояване), подобна на тази, която се наблюдава при аденоми на колона, може да се наблюдава към повърхността. Възпалението обикновено е минимално.
При високостепенната дисплазия (HGD) липсва повърхностно зреене. Може да се наблюдава струпване на цитологично (клетъчно) необичайни жлези или да е налице значително нарушена структура, с видими жлезни струпвания и минимално засягане на ламина проприя.
Ядрата са хиперхромни (по-интензивно оцветени) и са налице нарушения в ядрената мембрана. Клетките може да са или с деликатно струпване на тъмен хетерохроматин и незабележими нуклеоли, или с видими неправилни ядра с неравномерни струпвания на хроматина и нуклеоли с неправилна форма.
Значително уголемените хиперхромни клетки са характерна особеност на високостепенната дисплазия, като те могат да достигнат и до повърхността. При този вид дисплазия се наблюдава загуба на ядрена полярност, а митозите са лесно разпознаваеми.
Възпалението обикновено е минимално, но в някои случаи се наблюдава и значително възпаление.
В други случаи са налице множество малки жлези, разположени в един слой с хиперхромни ядра, вместо стратифицирани ядра. Този вид промени се означават като неаденоматозна дисплазия.
Налице са данни, според които едновременното откриване на високостепенна дисплазия и разязвяване е силно подозрително за инвазивен карцином.
Диагноза
Диагностицирането на високостепенната дисплазия може да стане само ако се намали възпалението чрез потискане на киселинната секреция.
Потвърждаването на високостепенна дисплазия трябва стане от поне двама опитни патолози. HGD носи основния риск за развитие на рак, дори при пациенти, които са били подложени на езофагектомия, като риска при тях е 40-75%.
Има някои данни, според които се предполага, че нискостепенната и високостепенната дисплазия могат да регресират.
Разграничаването между високостепенната дисплазия и най-ранната форма на интрамукозен (вътрелигавичен) карцином (дефиниран като инвазия през базалната мембрана до lamina propria или muscularis mucosae (мускуларис мукозе е един от подслоевете на лигавицата), но не и отвъд) е затруднено. Като цяло, при интрамукозния карцином се наблюдават:
- изменения в lamina propria и синцитиален модел на растеж;
- разширени жлези, които се разполагат непосредствено една до друга (гръб в гръб, back-to-back);
- смесване на единични клетки и малки групи от клетки в lamina propria;
През този етап обикновено не се наблюдава десмоплазия (образуване на съединителна тъкан). При карцином, който е инвазирал по-дълбоко (в субмукозата), десмоплазия и инфилтративен модел на растеж са добре изразени.
В горната част на гастроинтестиналния (стомашно-чревния) тракт инвазията в lamina propria е значително по-добре изразена, отколкото при дебелото черво, тъй като ламина проприя на дебелото черво няма изразена връзка с лимфни структури. Инвазията в ламина проприя при дебелото черво е еквивалентна на високостепенната дисплазия, докато при хранопровода може да доведе до метастазиране.
При Баретовия хранопровод се наблюдава замяна на нормалния плосък епител на хранопровода от цилиндричен епител. Метапластичният епител има плоска или ресничеста повърхност и е идентичен на стомашната чревна метаплазия от непълен тип (тип II или III). Метапластичната цилиндрична лигавица се класифицира в един от трите вида:
- повърхностен (кардиачен) тип лигавица;
- париетален тип мукоза (лигавица);
- специфичен, отличителен тип лигавица (наречена още специализирана Баретова лигавица или Баретова метаплазия). Това е лигавица, съдържаща цилиндрични клетки и чашковидни клетки, които нормално присъстват само в тънките черва и дебелото черво. Обикновено чашковидните клетки се смесват със стомашния тип покривни клетки, като този вид метаплазия се означава като непълна;
Специфичният тип Баретова лигавица е най-важен от тези три вида, като в действителност, в сегашната практика Баретовия хранопровод се отъждествява с наличието на този тип лигавица.
Чашковидните клетки се оцветяват с Алцианово синьо при ниско рН (2.5).
Макар и рядко, могат да се открият огнища на пълна чревна метаплазия (тип I) - с абсорбтивни клетки и клетки на Панет (Paneth).
Лигавичните жлези под повърхността на епитела също могат да съдържат метапластичен епител.
Скорошни проучвания показват, че метаплазията на цилиндричния епител произхожда от мултипотентни клетки (клетки, от които се развиват няколко други типове клетки), намиращи се в присъщите на хранопровода жлези.
TNM класификацията, използвана при плоскоклетъчния карцином, се прилага и при Баретов аденокарцином и може да осигури важни прогностични данни.
Епителната атипия при Баретовия хранопровод обикновено се преценява в зависимост от системата, създадена за оценка на атипията при улцерозен колит, а именно:
- отрицателен,
- положителен или
- неопределен резултат за интраепителна неоплазия;
Ако е налице интраепителна неоплазия, тя трябва да се класифицира като нискостепенна (синоним на лека до умерена дисплазия) или като високостепенна (синоним на тежка дисплазия или карцином in situ). Критериите, използвани за стадиране на интраепителната неоплазия, включват цитологични и структурни особености.
Интраепителната неоплазия при Баретовия хранопровод се определя като неопластичен процес, ограничен до епитела. Честотата й в Баретовата лигавица е приблизително 10% и се развива само в чревен тип метапластичен епител. Цитологичните аномалии обикновено достигат до повърхността на лигавицата.
Обикновено lamina propria на Баретовата лигавица съдържа придружаващ слабо изразен възпалителен инфилтрат от мононуклеарни (едноядрени) клетки. Може да са налице и леки реактивни промени, с уголемени и хипехромни ядра, добре изразени нуклеоли, а понякога и слабо изразена стратификация в долната част на жлезите, но въпреки това се наблюдава узряване на епитела към повърхността, с наличие на малко или никакви аномалии. Тези критерии отговарят на критериите за атипия, която е отрицателна за интраепителна неоплазия и обикновено могат да бъдат разграничени от нискостепенна интраепителна неоплазия.
При нискостепенната интраепителна неоплазия е налице:
- намалена секреция на мукус (слуз);
- ядрена псевдостратификация (лъжливо разслояване), ограничена до долната половина на жлезистия епител;
- митози (вид клетъчно делене);
- слабо изразен плеоморфизъм (променливост в размера, формата и оцветяването на ядрата);
- минимални промени в архитектурата;
Високостепенната интраепителна неоплазия се характеризира с:
- значителен плеоморфизъм и намалена секреция на слуз;
- висока митотична активност;
- ядрена стратификация, достигаща до горната част на клетките и жлезите;
- видни структурни аберации (отклонение от нормалния растеж и развитие). Най-тежките структурни промени се характеризират с крибриформени промени, които са характеристика на високостепенната интраепителна неоплазия до момента, до който не се наруши базалната мембрана на неопластичните жлези;
Интраепителната неоплазия обикновено няма характерни отличителни характеристики и се установява чрез системното вземане на проби от плосък Баретов епител.
Засегнатият район е изменчив, а също така често се срещат и множество огнища на дисплазия.
В някои случаи интраепителната неоплазия се представя като една или няколко нодуларни (възлести) маси, наподобяващи аденоми на широка основа (без краче).
Рядко, диспластични лезии са били считани за истински аденоми, с разширяващ се, но локализиран растеж, което води до образуването на добре разграничена от околните тъкани зона.
Едно от най-големите предизвикателства за патолозите при Баретовия хранопровод е разграничаването на интраепителна неоплазия от реактивни или регенеративни епителни промени. Това е особено трудно, а понякога дори невъзможно, ако са налице ерозии или язви.
В областите, граничещи с ерозии и язви, метапластичния епител може да демонстрира вилозна хиперплазия в повърхностните фовеоли (много малки ямички), с цитологичен (клетъчен) атипизъм и архитектурни нарушения. Тези нарушения обикновено са по-леки от тези, наблюдавани при интраепителна неоплазия. Налице е нормално разрастване на базалната (намираща се в основата) репликационна (репликация — етап от биосинтезата) зона в регенеративния епител, докато при интраепителната неоплазия пролиферацията води до разрастването на повече повърхностни епителни части.
Ако има съмнение за това дали реактивни и регенеративни промени или интраепителната неоплазия са налични в биопсичните проби, подходяща е категорията "атипия, неопределена за интраепителна неоплазия" и е наложително да се направи повторна биопсия, но след като се приложи контрол над рефлукса чрез потискането с медикаменти на киселинното производство или приложението на анти-рефлукс терапия.
Клинична картина
Баретовият хранопровод, като предшественик на повечето аденокарциноми, не причинява клинични симптоми в до 90% от случаите. Симптомите при Баретовия хранопровод, когато има такива, са като при гастроезофагеален рефлукс. Това е състояние, при което трябва да се търсят най-ранните етапи на неоплазия (интраепителна и интрамукозна неоплазия).
Диагноза
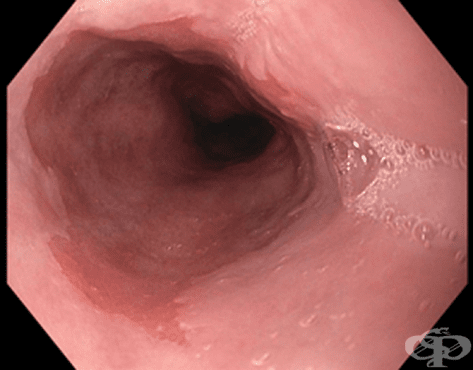
Ендоскопско изследване
Ендоскопски, ранните тумори могат да приличат на малки полиповидни, аденоматозно подобно лезии, но по-често са плоски, хлътнали, повдигнати или окултни (скрити), поради което се препоръчва вземането на тъканна проба, когато не е налице видима макроскопска промяна.
Ендоскопският анализ на сквамозно-цилиндричната граница (границата между плосък и цилиндричен епител) има за цел откриването на метаплазия в цилиндричния епител в дисталната (далечната) част на хранопровода. При ендоскопия се вижда, че сквамозно-цилиндричната граница (Z-линията) е разположена в гръдния кош, точно над диафрагмалния хиатус (отворът в диафрагмата, през който преминава хранопровода, за да достигне стомаха).
Ако дължината на лигавицата, съдържаща цилиндрични клетки, е 3 см в този дистален сегмент, състоянието се означава като Баретова метаплазия с дълъг сегмент, когато е < 3 см — метаплазия с къс сегмент.
Единични или множествени пръстовидни (1-3 см) издатини на цилиндричния епител се класифицират като къс тип метаплазия.
Пациентите, имащи Баретов хранопровод с къс сегмент (< 3 см), са по-малък риск за развитие на аденокарцином in situ, в сравнение с тези, които са с дълъг сегмент на Баретовия хранопровод.
Аденокарциномът на къс сегмент от Баретовия хранопровод лесно може да се сбърка с аденокарцином на кардията.
Тъй като аденокарцином in situ, произхождащ от дисталния хранопровод, може да проникне в кардията, а карцином на кардията или субкардиалната зона може да инвазира в дисталния хранопровод, тези образувания често са много трудни за разграничаване.
Когато наличието на Баретов хранопровод се ограничава до случаите с хистологично потвърдена чревна метаплазия, тогава е необходимо и вземането на подходящи тъканни проби.
При изследванията не е необходимо наличието на чашковидни клетки за диагностициране на Баретов хранопровод, като по този начин наличието на тази лигавица е повече ендоскопска, отколкото хистологична диагноза.
Пациентите със специфичен Баретов хранопровод са най-податливи на развитие на дисплазия и аденокарциноми.
Маркерите за дисплазия, които са били най-добре проучени, включват p53 (туморен протеин p53, Tumor protein p53) и Ki-67 (маркер за пролиферация Ki-67, marker of proliferation Ki-67), като и при двата се наблюдава усилена експресия (изява) при дисплазия. Освен тях, налице е и експресия на MUC1 (муцин 1, Mucin 1), MUC6, MUC5AC (муцин 5AC, mucin 5AC), както и MUC2.
Флоуцитометрия
Флоуцитометрията (лазерен метод за анализ на функционални и структурните характеристики на клетки или частици) и експресията на р53 спомагат за идентифицирането и проследяването на пациенти с най-висок риск или дори при идентифицирането на ендоскопски огнища при пациенти, които са подложени на ендоскопски скринингови програми. Грешното вземане на проби може да бъде сериозен проблем в наблюдението на тези пациенти, но използването на суправитално оцветяване (метод за оцветяване, използван в микроскопията за изследване на живи клетки, които са били отстранени от организма) или по-нови техники, като например конфокална лазерна ендоскопия или други методи, използвани за "оптична биопсия", улеснява избирането на най-подходящите места за биопсия.
Друг метод, който улеснява откриването на дисплазия, е оцветяването с метиленово синьо. Метиленовото синьо обагря интестиналната (чревната) метаплазия и има доказателства, че чрез този метод се редуцира броя на необходимите биопсии, освен това струва по-евтино и по-често открива диспластични промени и аденокарциноми, в сравнение с другите методи.
Прогноза
Аденокарциномът на хранопровода има лоша прогноза, като шансовете се увеличават, ако се предприемат действия за отстраняването му и намаляват, ако остане неопериран. Препоръчва се пациентите, които са със симптоми на рефлукс от дълго време, особено ако са над 50-годишна възраст, да се подложат на скринингова ендоскопия, като се търсят промени, характерни за Баретов хранопровод. При ендоскопията се вземат биопсии от четири участъка на интервал от 2 см.
Аденокарциномите, които произлизат от Баретов хранопровод, метастазират към параезофагеалните (намиращи около хранопровода) и паракардиалните (разположени в областта на кардията) лимфни възли, лимфните възли по малката кривина на стомаха, както и към целиачните (трункус целиакус — първият голям клон на коремната аорта) лимфни възли. Далечни метастази се появяват по-късно.
Лечение
В миналото е била препоръчвана езофагектомия (хирургично отстраняване на хранопровода) при високостепенната дисплазия, но това вече не е така. В настоящия момент са налице много положителни данни за прилагането на ендоскопска аблация посредством фотодинамична терапия, радиочестотна аблация, както и ендоскопска резекция (пълно или частично изрязване на тъкан или орган) на лигавицата.
Коментари към Карцином in situ на хранопровод МКБ D00.1